DE oplosbaarheid, of oplosbaarheidscoëfficiënt, het is een fysieke eigenschap van materie die praktisch altijd in het laboratorium wordt bepaald. Het is gerelateerd aan de capaciteit die een materiaal, genaamd opgeloste stof, cadeautjes die door een ander moeten worden opgelost, de oplosmiddel.
Wat de oplosbaarheid betreft, kunnen opgeloste stoffen als volgt worden ingedeeld:
Oplosbare stoffen: die oplossen in het oplosmiddel. Natriumchloride (opgeloste stof) is bijvoorbeeld oplosbaar in water (oplosmiddel);
Licht oplosbaar: die moeite hebben met oplossen in het oplosmiddel. Dit is het geval van calciumhydroxide [Ca(OH)2] (opgeloste stof) in water;
onoplosbare stoffen: die lossen niet op in het oplosmiddel. Zand (opgeloste stof) is bijvoorbeeld onoplosbaar in water.
DE oplosbaarheid wordt sterk geassocieerd met de voorbereiding van oplossingen (homogene mengsels), aangezien het voor het verkrijgen van een oplossing essentieel is dat de gebruikte opgeloste stof oplosbaar is in het oplosmiddel.
Factoren die de oplosbaarheid beïnvloeden
Zelfs wanneer de opgeloste stof oplosbaar is in het oplosmiddel, zijn er enkele factoren die het vermogen van de opgeloste stof om op te lossen kunnen beïnvloeden. Zijn zij:
a) Relatie tussen de hoeveelheid opgeloste stof en oplosmiddel
Het oplosmiddel heeft altijd een limiet aan opgeloste stof die het kan oplossen. Als we de hoeveelheid oplosmiddel verhogen met behoud van de hoeveelheid opgeloste stof, heeft het oplosmiddel de neiging om alle gebruikte opgeloste stof op te lossen.
B) Temperatuur
Temperatuur is de enige fysieke factor die de oplosbaarheid van een oplosmiddel ten opzichte van een bepaalde opgeloste stof kan wijzigen. Deze wijziging hangt af van de aard van de opgeloste stof, zoals we hieronder zullen zien:
endotherme opgeloste stof: is degene die we erin slagen een grotere massa op te lossen, zolang het oplosmiddel een temperatuur heeft die hoger is dan kamertemperatuur. Hoe heter het oplosmiddel, hoe meer opgeloste stof zal oplossen.
Voorbeeld: Het is mogelijk om een grotere hoeveelheid gemalen koffie op te lossen als het water heet is.
Exotherme opgeloste stof: is degene die we erin slagen een grotere massa op te lossen, zolang het oplosmiddel een temperatuur heeft die lager is dan kamertemperatuur. Hoe kouder het oplosmiddel, hoe meer opgeloste stof zal oplossen.
Voorbeeld: Het is mogelijk om een grotere hoeveelheid kooldioxide op te lossen als de frisdrank koud is.
Manieren om de oplosbaarheid te bepalen
Omdat de oplosbaarheid een eigenschap is die op een experimentele manier is bepaald, is de oplosbaarheid van de materialen in het algemeen al in de meest verschillende oplosmiddelen beoordeeld. We kunnen dus als volgt toegang krijgen tot de oplosbaarheid van een opgeloste stof in een bepaald oplosmiddel:
a) Analyse van een tabel
Vaak kan de student oplosbaarheid tegenkomen bij de interpretatie van een tabel. Zie het volgende voorbeeld:
Voorbeeld: (UEPG - aangepast) Onderstaande tabel toont de oplosbaarheid van Li-zout2CO3 op 100 gram water.
Niet stoppen nu... Er is meer na de reclame ;)

De tabel presenteert de massawaarden in gram Li2CO3 die kan worden opgelost in 100 gram water, vanaf 0 OC tot 50 O. We kunnen zien dat hoe heter het water, hoe minder Li2CO3 lost op. Daarom, Li2CO3 het is een exotherme opgeloste stof (het zal meer oplossen als het water koud is).
b) Analyse van een grafiek
De oplosbaarheid kan worden beoordeeld door een grafiek te interpreteren. Om dit te doen, bepaalt u eenvoudig de temperatuur, draait u deze naar de curve en draait u de curve vervolgens naar de y-as, de massa in grammen opgeloste stof die zal worden opgelost.
Voorbeeld: (UFTM - aangepast) De grafiek toont de oplosbaarheidscurve van een AX-zout2.
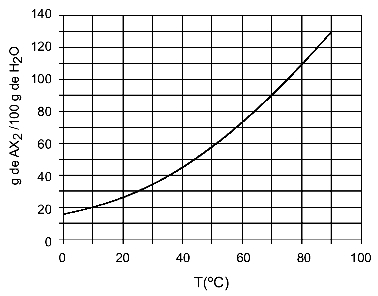
In de grafiek staat dat op de y-as de hoeveelheid water (oplosmiddel) 100 gram is. Voor opgeloste stof AX2, zullen we de hoeveelheid water bepalen bij de volgende temperaturen:
30O: Wanneer we de temperatuur 30. inschakelenOC naar de curve en dan de curve naar de y-as, we hebben dat bij deze temperatuur de 100 gram water ongeveer 35 gram opgeloste stof AX kan oplossen2.
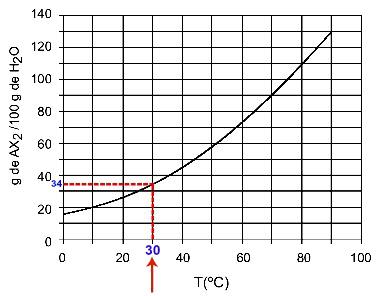
Bepaling van AX-oplosbaarheid2 bij 30OÇ
40O: Wanneer we de temperatuur 40. inschakelenOC naar de curve en dan de curve naar de y-as, we hebben dat bij deze temperatuur de 100 gram water ongeveer 45 gram opgeloste stof AX kan oplossen2.
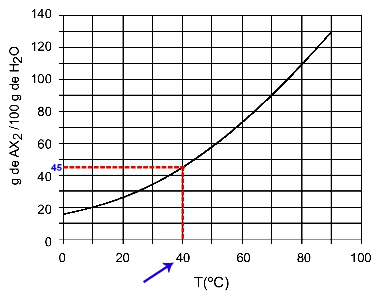
Bepaling van AX-oplosbaarheid2 bij 40OÇ
Omdat de opgeloste hoeveelheid opgeloste stof groter is bij elke temperatuurstijging, hebben we dat de AX2 het is een endotherme opgeloste stof.
c) tekstuele interpretatie
Zie het volgende voorbeeld:
Voorbeeld: (PUC-MG) Bepaalde stoffen kunnen homogene mengsels vormen met andere stoffen. De stof die in de grootste hoeveelheid aanwezig is, wordt een oplosmiddel genoemd en de stof die in de kleinste hoeveelheid aanwezig is, wordt een opgeloste stof genoemd. Natriumchloride (NaCl) vormt met water een homogene oplossing, waarin bij 20C 36 g NaCl in 100 g water kan worden opgelost.
In de tekst staat dat als we 100 gram water (oplosmiddel) bij een temperatuur van 20 OC is het mogelijk om tot 36 gram NaCl op te lossen.
Door mij Diogo Lopes Dias
Wil je naar deze tekst verwijzen in een school- of academisch werk? Kijken:
DAGEN, Diogo Lopes. "Wat is oplosbaarheid?"; Brazilië School. Beschikbaar in: https://brasilescola.uol.com.br/o-que-e/quimica/o-que-e-solubilidade.htm. Betreden op 28 juni 2021.