geometrische isomeer is een soort van ruimte isomerie die de positie in de ruimte van de liganden van twee koolstofatomen in een keten evalueert en vergelijkt. Deze evaluatie wordt gemaakt vanuit een denkbeeldig vlak tussen de betrokken koolstoffen.
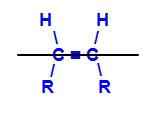
Denkbeeldig vlak dat het molecuul verdeelt
Het denkbeeldige vlak in de structuur hierboven verdeelt het molecuul in een bovenvlak en een ondervlak. Hiermee kunnen we de koolstofliganden die bij elk van deze vlakken betrokken zijn, evalueren en vergelijken. Zie de soorten geometrische isomeren:
→ Cis-trans geometrische isomeer
Een verbinding heeft cis-trans geometrische isomerie wanneer de ketting het volgende weergeeft:
Open keten met een dubbele binding tussen twee koolstofatomen, die dezelfde linkers aan elkaar hebben. Zie een voorbeeld:
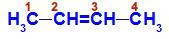
Structuurformule van But-2-een
In de structuur kunnen we zien dat zowel koolstof 2 als koolstof 3 dezelfde liganden hebben, namelijk waterstof (H) en methyl (CH3).
Gesloten keten met twee koolstoffen die dezelfde liganden aan elkaar hebben. Zie een voorbeeld:
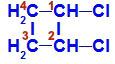
Structuurformule van 1,2-dichloorcyclobutaan
In de structuur kunnen we zien dat zowel koolstof 1 als koolstof 2 dezelfde liganden hebben, namelijk waterstof (H) en chloor (Cl).
Om cis-trans isomerie uit te leggen, gebruiken we but-2-een:
a) Cis-isomeer: is de geometrische isomeer waarin dezelfde liganden hetzelfde vlak bezetten. In het onderstaande voorbeeld bevinden de waterstofatomen zich in hetzelfde vlak, evenals de methylradicalen.

Structuurformule van cis-but-2-een
b) Trans-isomeer: is de geometrische isomeer waarin verschillende liganden hetzelfde vlak bezetten. In het onderstaande voorbeeld hebben we op hetzelfde vlak een waterstof en een methyl (CH3).
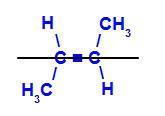
Structuurformule van trans but-2-eenen
Niet stoppen nu... Er is meer na de reclame ;)
→ E-Z geometrische isomeer
Een verbinding heeft E-Z geometrische isomerie wanneer de keten heeft:
Open keten met een dubbele binding tussen twee koolstofatomen, die alle of enkele verschillende linkers hebben. Zie een voorbeeld:
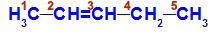
Structuurformule van pent-2-een
In de structuur kunnen we zien dat koolstof 2 het methylligand heeft (CH3) en waterstof (H), en koolstof 3 heeft de waterstof (H) en ethyl (H) ligand3C-CH2).
Gesloten keten met twee koolstoffen die alle of sommige liganden van elkaar verschillen. Zie een voorbeeld:
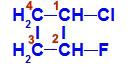
Structuurformule van 1-chloor-2-fluorcyclobutaan
In de structuur kunnen we zien dat koolstof 1 waterstof en chloor heeft als de belangrijkste liganden, en koolstof 2 heeft waterstof en fluor als de belangrijkste liganden.
OPMERKING: Van de verschillende liganden, in geometrische isomerie, evalueren we de complexiteit van het ligand (aantal atomen) of het atoomnummer.
Om het E-Z-isomeer uit te leggen, zullen we zowel pent-2-een als 1-chloor-2-fluor-cyclobutaan gebruiken:
a) E-isomeer
geometrische isomeer waarin de meer complexe liganden of die met het grootste atoomnummer op tegenovergestelde vlakken zijn geplaatst. In het volgende voorbeeld is het meest complexe ligand op koolstof 2 methyl, en het meest complexe ligand op koolstof 3 is ethyl, die zich op verschillende vlakken bevinden.
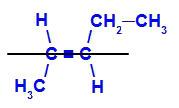
Structuurformule van E-pent-2-een
b) Isomeer Z
geometrische isomeer waarbij de meer complexe liganden of die met het hoogste atoomnummer zich op hetzelfde vlak bevinden. In het volgende voorbeeld is het ligand met het hoogste atoomnummer van koolstof 1 chloor (Z = 17), en het ligand met het hoogste atoomnummer van koolstof 2 is fluor (Z = 9), die zich in hetzelfde vlak bevinden.
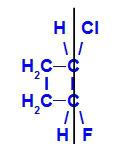
Structuurformule van Z-1-chloor-2-fluorcyclobutaan
Door mij Diogo Lopes Dias
Wil je naar deze tekst verwijzen in een school- of academisch werk? Kijken:
DAGEN, Diogo Lopes. "Wat is geometrische isomerie?"; Brazilië School. Beschikbaar in: https://brasilescola.uol.com.br/o-que-e/quimica/o-que-e-isomeria-geometrica.htm. Betreden op 28 juni 2021.
Chemie
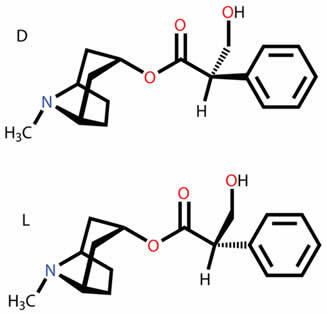
Weet waar de verschillende soorten vlakke en ruimtelijke isomeren over gaan, zoals functie, positie, keten, tautomerie, metamerie, cis-trans geometrische en optische isomerie.