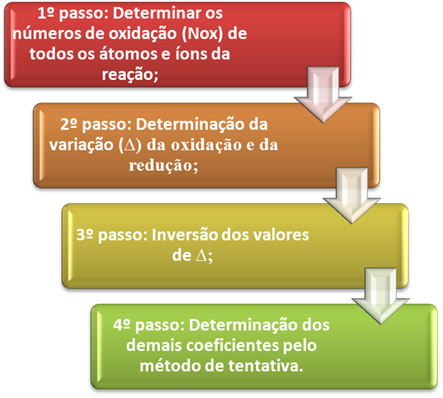
Om een chemische reactie te laten plaatsvinden, moet aan vier basisvoorwaarden worden voldaan, namelijk:
1. Er moet contact worden opgenomen met reagentia;
2. Er moet chemische affiniteit zijn tussen de reagentia;
3. Botsingen tussen reagensdeeltjes moeten effectief zijn;
4. Activeringsenergie moet worden bereikt.
Bekijk elk geval kort:
1.Contact tussen reagentia:
Deze voorwaarde is duidelijk, want zelfs als de reactanten veel affiniteit met elkaar hebben, zoals in het geval van zuren en basen, zal de reactie niet plaatsvinden als ze worden gescheiden. Ze moeten met elkaar in contact komen zodat hun deeltjes kunnen botsen, de bindingen van de reactanten verbreken en de bindingen van de producten vormen.

2.Chemische affiniteit:
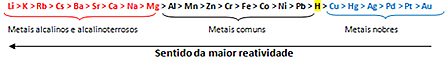
Zoals we hebben gezien, is het nodig om de reagentia met elkaar in contact te brengen, maar niet genoeg. Als we bijvoorbeeld natrium in contact brengen met water, ontstaat er een extreem heftige reactie, maar als we goud plaatsen, zien we geen verschil. Dit komt omdat verschillende stoffen verschillende chemische affiniteiten met elkaar hebben, of helemaal geen affiniteit hebben. Hoe groter de chemische affiniteit, hoe sneller de reactie.
In de genoemde voorbeelden heeft natrium een grote affiniteit met water, zozeer zelfs dat om niet in contact te komen met het vocht in de lucht, metallisch natrium wordt opgeslagen in kerosine. Goud is inert, daarom gaan gouden monumenten zo lang mee, zoals de sarcofagen van Egypte.

3.Botsingstheorie:
Zelfs in verbindingen die chemische affiniteit hebben, is het nodig dat hun deeltjes, atomen of moleculen effectief botsen om de reactie te laten verlopen. Niet alle deeltjes die botsen doen dit effectief, maar schokken die resulteren in het breken van de reagensbindingen en vorming van nieuwe bindingen zijn die bindingen die plaatsvinden in de juiste richting en met de energie genoeg.
Niet stoppen nu... Er is meer na de reclame ;)
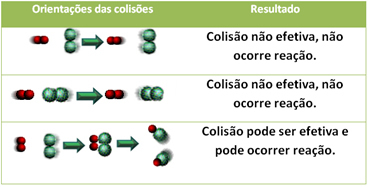
Hieronder wordt het geval weergegeven van twee ineffectieve botsingen en één effectieve botsing die resulteert in de reactie.
4.Activeringsenergie en geactiveerd complex:
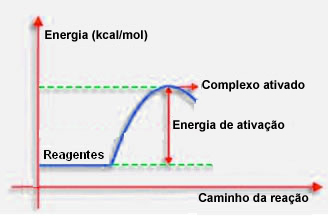
Zoals in het vorige item vermeld, heeft een effectieve aanrijding, naast een gunstige begeleiding, ook voldoende energie nodig. De minimale hoeveelheid energie die nodig is om elke reactie te laten plaatsvinden, wordt de activeringsenergie genoemd.
Als de reactanten een energie hebben die gelijk is aan of groter is dan de activeringsenergie, tijdens de goed georiënteerde schok, er zal zich een aanvankelijk geactiveerd complex vormen, dat een intermediaire structuur is tussen de reactanten en de producten. In het geactiveerde complex zijn er verzwakte reagensbindingen en vormen zich nieuwe productbindingen.
De activeringsenergie werkt dus als een soort barrière voor de reactie, want hoe groter deze is, hoe moeilijker het zal zijn voor de reactie. In sommige gevallen is het nodig om de reagentia van energie te voorzien. Kookgas heeft bijvoorbeeld een affiniteit voor interactie met zuurstof in de lucht, maar we moeten energie leveren als we de lucifer bij elkaar brengen, anders vindt de reactie niet plaats. Maar eenmaal begonnen, geeft de reactie zelf genoeg energie vrij om de andere moleculen te activeren en de reactie gaande te houden.
Door Jennifer Fogaça
Afgestudeerd in scheikunde
Wil je naar deze tekst verwijzen in een school- of academisch werk? Kijken:
FOGAÇA, Jennifer Rocha Vargas. "Voorwaarden voor het optreden van chemische reacties"; Brazilië School. Beschikbaar in: https://brasilescola.uol.com.br/quimica/condicoes-para-ocorrencia-reacoes-quimicas.htm. Betreden op 27 juni 2021.