Sommige verbindingen hoeven geen acht elektronen in de valentieschil te hebben om stabiliteit te bereiken, dus worden ze beschouwd als uitzonderingen op de Octet-regel. Ontdek nu waarom sommige elementen ontsnappen aan de verplichting om een octet van elektronen in de laatste schil te hebben.
Beryllium (Worden)
Het is een uitzondering op de Octet-regel omdat het verbindingen kan vormen met twee enkele bindingen, dus het stabiliseert met slechts vier elektronen in de valentieschil. 
Omdat waterstof (H) twee elektronen moet afstaan om de binding te maken (H - Nou - H), deelt het Beryllium (Be)-atoom zijn elektronen en bereikt het stabiliteit.
Aluminium (Al)
Het is een uitzondering op de Octet-regel omdat het stabiliteit bereikt met zes elektronen in de valentieschil. Het aluminiumatoom heeft de neiging zijn elektronen af te staan en kan dus drie enkele bindingen vormen met andere atomen: 
In dit geval vormde aluminium (Al) drie bindingen met drie fluor (F) -atomen.
borium (B)
Het vormt moleculaire stoffen met drie enkele bindingen.
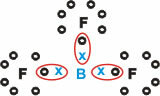
Merk op dat boor (B) de neiging heeft zijn elektronen af te staan aan fluor (F) -atomen, wat de Octet-regel gehoorzaamt, waarbij acht elektronen in de valentieschil nodig zijn. Terwijl boor zijn elektronen afstaat, stabiliseert fluor zich met het gevormde octet.
Door Liria Alves
Afgestudeerd in scheikunde
Brazilië School Team
Bekijk meer!
Octettheorie
Algemene scheikunde - Chemie - Brazilië School
Bron: Brazilië School - https://brasilescola.uol.com.br/quimica/excecoes-regra-octeto.htm

