We zullen in deze tekst zien hoe a grafiek van verandering van fysieke toestand aan wie dan ook pure substantie, hoe dit type diagram moet worden geïnterpreteerd en hoe de grafiek van mengsels wordt weergegeven.
Laten we hiervoor het voorbeeld van water bekijken. Stel je voor dat we een glas ijs van –10 ºC nemen en een verwarmingsproces starten, onder een druk van 1 atm. Naarmate de temperatuur stijgt, van -10 ºC naar -9 ºC, naar -8 ºC enzovoort, blijft het ijs in vaste toestand totdat het een temperatuur van 0 ºC bereikt.
Op dit punt begint het te veranderen in een vloeibare toestand, dat wil zeggen dat fusie begint plaats te vinden. De temperatuur zal niet verder stijgen zoals voorheen, maar zal constant op 0°C blijven totdat al het ijs is gesmolten:

Nadat alle vaste stoffen zijn gesmolten, zal de temperatuur van het systeem blijven stijgen tot een temperatuur van 100°C. Bij deze temperatuur zal het water dat zich in vloeibare toestand bevond, beginnen te veranderen in de damptoestand, dat wil zeggen, het zal koken.
Net zoals het gebeurde in de fusiepunt, bij het kookpunt zal de temperatuur ook constant blijven totdat alle vloeistof in damp verandert. Als we het systeem daarna blijven verwarmen, zal de temperatuur blijven stijgen:
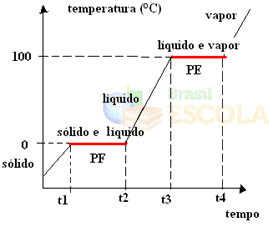
Klaar! Dit is de grafiek of het diagram dat de verandering in de fysieke toestand van water of zijn verwarmingscurve weergeeft. Als het het omgekeerde proces zou zijn, zouden we de volgende waterkoelingscurve hebben:
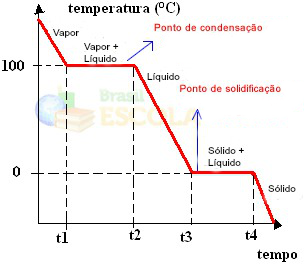
Een heel belangrijk aspect van deze grafieken is dat ze worden gevormd door twee niveaus, dat wil zeggen dat er twee punten zijn waar de temperatuur een tijdje constant blijft. Dit gebeurt altijd bij de verandering van toestand van een zuivere stof. Het enige verschil zijn de smelt- en kookpuntwaarden.
Zuurstof is bijvoorbeeld, in tegenstelling tot water, geen vloeistof, maar een gas bij kamertemperatuur (ongeveer 20ºC). Dit komt omdat het smeltpunt op zeeniveau -223,0 °C is en het kookpunt -183,0 °C. Zie uw fysieke toestandsveranderingsgrafiek:

Gemeenschappelijke mixafbeeldingen
Als we een mengsel verwarmen of koelen, hebben het smeltpunt en het kookpunt geen bepaalde en constante waarden, dat wil zeggen dat de twee niveaus die in de grafieken worden waargenomen, niet worden gevormd bovenstaande.
Veranderingen in fysieke toestanden zullen optreden over temperatuurbereiken in plaats van een vaste hoeveelheid. Het smeltpunt begint bijvoorbeeld bij een bepaalde temperatuur en eindigt bij een andere, en hetzelfde zal gebeuren met het kookpunt, zoals weergegeven in de volgende grafiek:
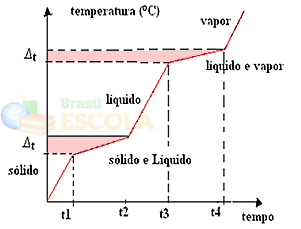
Twee uitzonderingen zijn eutectische en azeotrope mengsels. Kijk wat er met hen gebeurt:
a) Eutectisch mengsel
Het eutectische mengsel gedraagt zich tijdens de fusie alsof het een zuivere stof is, d.w.z. op dat moment blijft de temperatuur constant van het begin tot het einde van de verandering van aggregatietoestand.

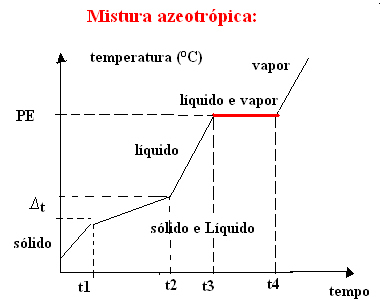
b) azeotroop mengsel
Het azeotropische mengsel gedraagt zich tijdens het koken als een zuivere stof, dat wil zeggen dat de temperatuur op dit punt constant blijft van het begin tot het einde van de verandering in aggregatietoestand.
Door Jennifer Fogaça
Afgestudeerd in scheikunde
Bron: Brazilië School - https://brasilescola.uol.com.br/quimica/graficos-mudanca-estado-fisico.htm
