Nitroverbinding is een organische verbinding afgeleid van de chemische reactie tussen salpeterzuur (HNOH3) het is een alkaan (verzadigde koolwaterstof met open keten) of een aromatische stof. Wanneer salpeterzuur reageert met alkaan of aromatisch, treedt er een substitutiereactie op waarbij het zuur een hydroxylgroep (OH) verliest en de organische verbinding een waterstof verliest:
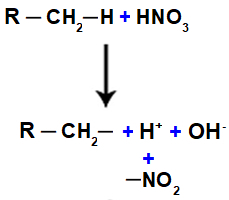
Vervolgens hebben we de vorming van een watermolecuul, resulterend uit de vereniging tussen OH en H, terwijl de GEEN groep2 (die overblijft van het zuur) bindt aan het alkaan of aromatische, vormen de nitroverbinding.
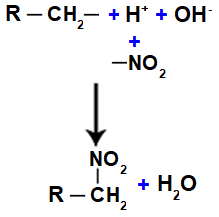
Vertegenwoordiging van de vorming van water en nitroverbindingen
Dus het belangrijkste structurele kenmerk van a nitroverbinding is de aanwezigheid van een of meer nitro groepen (BIJ DE2) gekoppeld aan een alkaan of een aromatisch.
eigendommen
Rekeninghoudend met eigendommen fysiek, kunnen we benadrukken:
Over het algemeen zijn het bij kamertemperatuur stroperige vloeistoffen (met uitzondering van nitroverbindingen met een lage molmassa, die vloeibare vloeistoffen zijn);
Ze hebben hoge smelt- en kookpunten;
Ze zijn dichter dan water;
Over het algemeen zijn ze onoplosbaar in water, met uitzondering van nitromethaan en nitroethaan;
Wanneer ze worden gevormd door een alifatische keten, hebben ze een aangenaam aroma en zijn ze niet giftig. Nu, als ze worden gevormd door een aromatische keten, zijn ze giftig en hebben ze een onaangenaam aroma;
O type intermoleculaire kracht dat zijn moleculen verenigt is de permanente dipool, omdat ze polaire kenmerken hebben.
Met betrekking tot chemische eigenschappen moeten we weten dat de nitroverbindingen ze zijn zeer reactief, dat wil zeggen, ze worden gebruikt in verschillende organische reacties, zoals substitutiereacties.
De officiële nomenclatuurregel, voorgesteld door de IUPAC (International Union of Pure and Applied Chemistry), voor: nitroverbindingen é:
Nitro + voorvoegsel + tussenvoegsel + o
Opmerking: Het voorvoegsel is gerelateerd aan het aantal koolstoffen dat aanwezig is in de nitroverbindingsketen. Het tussenvoegsel is gerelateerd aan het type bindingen dat aanwezig is tussen koolstoffen.
Voorbeelden:
Nomenclatuur van een nitroverbinding met normale keten chain

In eerste instantie is het interessant om de string van te nummeren nitroverbinding (altijd van de koolstof die het dichtst bij de koolstof zit met de nitrogroep):
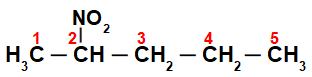
Door de string van de te nummeren nitroverbinding, we hebben daarin vijf koolstofatomen (prefix pent), alleen enkele bindingen tussen de koolstoffen (infix an) en de nitrogroep op koolstof 2. De naam van deze structuur is 2-nitropenthaan.
Nomenclatuur van een nitroverbinding met normale keten chain
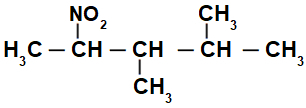
Structuurformule van een vertakte nitroverbinding
In eerste instantie is het interessant om de string van te nummeren nitroverbinding (altijd van de koolstof die zich het dichtst bij de koolstof bevindt met de nitrogroep) naar het uiteinde met het hoogste aantal koolstoffen voor de hoofdketen:
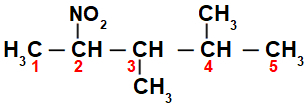
Door de string van de te nummeren nitroverbinding, we hebben dat daarin 5 koolstofatomen zijn (prefix pent), alleen enkele bindingen tussen de koolstoffen (infix an), twee methylradicalen (op koolstofnummers 3 en 4) en de nitrogroep op koolstof 2. De naam van deze structuur is 3,4-dimethyl-2-nitropentaan.
Toepassingen
U nitro verbindingen, in het algemeen kunnen ze worden gebruikt bij de vervaardiging van pesticiden, kleurstoffen, aniline, bactericiden, fungiciden, additieven, oplosmiddelen; ze fungeren ook als explosieven en bij olieraffinage.
Door mij Diogo Lopes Dias
Bron: Brazilië School - https://brasilescola.uol.com.br/o-que-e/quimica/o-que-e-nitrocomposto.htm

