O vinylchloride het is een koolwaterstof giftige gechloreerde en kankerverwekkende werking. Het is een kleurloos gas bij kamertemperatuur, zeer brandbaar en gevoelig voor hitte.
Het is het monomeer dat wordt gebruikt bij de vervaardiging van polyvinylchloride, een stof die bekend staat als PVC. O Pvc is een hittebestendige thermoplast (in tegenstelling tot zijn monomeer) die tal van toepassingen kent in de dagelijks leven, zoals het coaten van elektriciteitsdraden, aanleg van leidingen en diverse soorten verpakking.
Lees ook:Asbest - natuurlijke vezel met brede industriële toepassing, maar uiterst giftig voor mensen
Onderwerpen van dit artikel
- 1 - Samenvatting over vinylchloride
- 2 - Eigenschappen van vinylchloride
- 3 - Wat is vinylchloride?
- 4 - Kenmerken van vinylchloride
- 5 - Waar wordt vinylchloride voor gebruikt?
- 6 - Vinylchloride verkrijgen
-
7 - Voorzorgsmaatregelen met vinylchloride
- Vinylchloride en kanker
- 8 - Optreden van vinylchloride
- 9 - Geschiedenis van vinylchloride
Samenvatting over vinylchloride
Vinylchloride is een gechloreerde koolwaterstof met de formule H2C=CHCl.
Het is een gas kleurloos, zoetgeurend en licht ontvlambaar.
Vinylchloride is onstabiel warmte, in ontbinding.
De belangrijkste toepassing van vinylchloride is de vervaardiging van polyvinylchloride (PVC).
PVC is een thermoplast met tal van toepassingen, zoals leidingen, onderdelen, coatings, verpakkingen, etc.
Vinylchloride is giftig en heeft een kankerverwekkende werking.
vinylchloride eigenschappen
moleculaire formule: CH2CHCl (C2H3Kl).
Moleculaire massa: 62.498 gr/mol.
fysieke toestand: gas (kleurloos en met een sterke geur).
Dikte: 0,91 g/ml.
Oplosbaarheid in water: zeer slecht oplosbaar (0,6 g in 100 ml water, 20 °C).
smelttemperatuur: -154°C.
Kooktemperatuur: -13°C.
Niet stoppen nu... Er is meer na de publiciteit ;)
Wat is vinylchloride?
Vinylchloride is een gechloreerde koolwaterstof met de formule H2C=CHCl. Bij kamertemperatuur gebeurt het met a Kleurloos en licht ontvlambaar gas.
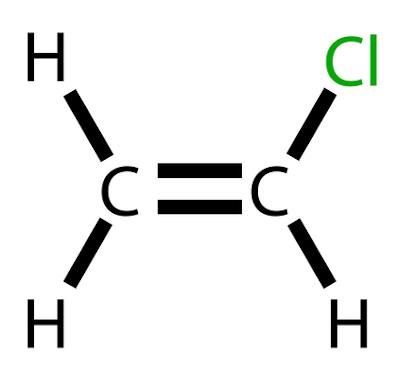
Vinylchloride, ook wel chlooretheen of vinylchloridemonomeer genoemd, is een chemisch product van groot belang in industrie, met een speciale toepassing bij de vervaardiging van polymeer polyvinylchloride, beter bekend als PVC. Deze verbinding bezet de lijst van de 20 afgeleide producten Aardolie van groter industrieel en economisch belang.
Lees ook:Benzopyreen - kankerverwekkende koolwaterstof die voorkomt in sigarettenrook en gegrild vlees
Kenmerken van vinylchloride
Vinylchloride is een Kleurloos gas met een milde, zoete geur. Het heeft de eigenschap licht ontvlambaar te zijn.
Bij blootstelling aan warmtebronnen, kunnen ontbinden, waarbij giftige dampen vrijkomen in kooldioxide, koolmonoxide, waterstofchloride en fosgeen. Omdat het een organische verbinding is, is de oplosbaarheid in water extreem laag, aan de andere kant is het oplosbaar in stoffen zoals ethanol, benzeen en tetrachloorkoolstof.
In aanwezigheid van vocht wordt vinylchloride bijtend en kan het de ijzer en de staal. Het heeft het vermogen om te polymeriseren wanneer het wordt blootgesteld aan hitte in atmosferische lucht, door middel van een exotherme reactie. Deze eigenschap ontleent veel van zijn industriële toepassingen.
Vinylchloride vraagt om aandacht omdat het is giftig en kankerverwekkend.
Waar wordt vinylchloride voor gebruikt?
Vinylchloride is de monomeer gebruikt om PVC-polymeer te vervaardigen (polyvinylchloride) en andere gechloreerde oplosmiddelen.
PVC is een thermoplast die wordt gebruikt bij de vervaardiging van verpakkingen, schoeisel, elektrische aansluitingen en kabels, pijpen, ramen, slangen en bloedafnamezakken, kledingstukken, onder talloze andere artikelen.

O PVC wordt gevormd door de polymerisatie van vinylchloride. In dit chemische proces voegt een groot aantal vinylchloridemoleculen zich aan elkaar toe en vormt zo een grote chemische structuur.
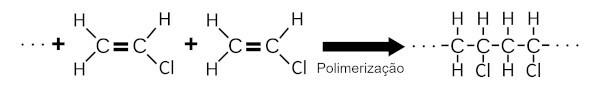
O PVC is vlamvertragend en om deze reden wordt het veel gebruikt in het coaten van draden, elektrische kabels en residentiële coatings.
Hoewel vinylchloride een chemische verbinding is die aandacht vereist vanwege zijn toxiciteit en thermische instabiliteit, het PVC-polymeer is zeer bestand tegen warmtebronnen, het is niet giftig en kan worden opgeslagen met veiligheid.
Tot 1974 werd vinylchloride gebruikt in spuitbussen. In het verleden werd het zelfs gebruikt als inhalatieverdoving. Met de kennis van de toxiciteit van deze verbinding werden deze toepassingen stopgezet.
Vinylchloride verkrijgen
De synthese van vinylchloride die op industriële schaal wordt gebruikt, is gestart met de verbinding ethyleen of etheen (CH2=CH2) en kan plaatsvinden via twee routes.
In de eerste wordt ethyleen omgezet in 1,2-dichloorethaan door reactie met chloorgas. Vervolgens wordt door verhitting van het 1,2-dichloorethaan in aanwezigheid van een katalysator vinylchloride verkregen als het hoofdproduct en het zoutzuur als secundair product.
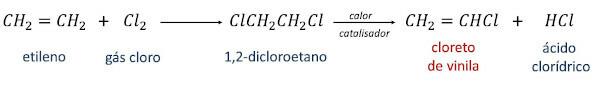
Bij de tweede reactieroute, bekend als oxychlorering, is de reactie tussen ethyleen, zoutzuur en zuurstof uit de atmosfeer zelf, in aanwezigheid van warmte en een katalysator, waarbij vinylchloride en water als producten worden gegenereerd.

Gewoonlijk wordt een productiecentrum voor vinylchloride gebouwd om beide productieprocessen te accommoderen. geciteerd, zodat het zoutzuur dat bij de eerste methode wordt gegenereerd, als reagens fungeert voor het uitvoeren van de tweede route.
Voorzorgsmaatregelen met vinylchloride
Vinylchloride is een giftige verbinding. Aangezien het een gas is, De belangrijkste vorm van besmetting is door inademing., daarom moet de behandeling ervan altijd gebeuren met behulp van geschikte apparatuur, zoals gasmaskers.
Blootstelling aan deze stof beïnvloedt de zenuwstelsel perifere en centrale, waardoor schade aan de lever. A Continue blootstelling kan het fenomeen van Raynaud veroorzaken, wat een reeks symptomen is, waaronder gewrichts- en spierpijn en huidveranderingen, die kunnen leiden tot een volledig verlies van huidelasticiteit, zelfs organen inwendige organen en bloedvaten.
Andere effecten zijn euforie, desoriëntatie, miskraam en geboorteafwijkingen. Verwondingen aan oogweefsel worden ook geregistreerd.
Symptomen zijn afhankelijk van het niveau van blootstelling aan de stof, variërend van duizeligheid, misselijkheid, visusstoornissen, hoofdpijn en ataxie bij acute blootstelling (van 1000 tot 8000 ppm vinylchloride in lucht), tot narcotisch effect, hartritmestoornissen en fatale ademhalingsinsufficiëntie bij blootstelling aan niveaus boven 12000 ppm.
Vinylchloride en kanker
O vinylchloride is een kankerverwekkende stof, geassocieerd met een hoog risico op het ontwikkelen van leverkanker, wat kan bijdragen aan het optreden van hersenkanker en longen, evenals kanker van het lymfestelsel.
Lees ook:Ammoniumnitraat — verbinding die in de landbouw wordt gebruikt en die explosies kan veroorzaken
Voorkomen van vinylchloride
het vinylchloride wordt spontaan gegenereerd in de omgeving door de ontleding van sommige verbindingen die bevatten chloordoor de werking van micro-organismen. Daarom kan het worden beschouwd als een lucht- en waterverontreiniging, vooral in regio's in de buurt stortplaatsen.
Vinylchloride komt echter het meest voor via synthetische routes, gerelateerd aan de chemische industrie, zoals eerder besproken.
Geschiedenis van vinylchloride
Vinylchloride was ontdekt in 1835 door de Duitse chemicus Justus von Liebig, bij het laten reageren van dichloorethaan met kaliumhydroxide in een alcoholische omgeving.
Later, in 1872, observeerde de chemicus Eugen Baumann voor het eerst de polymerisatie van vinylchloride, afkomstig van PVC, nadat hij per ongeluk een container met de stof had achtergelaten die aan de zon was blootgesteld.
In 1926 ontdekte de Amerikaanse uitvinder Waldo Semon chemische additieven die PVC meer elasticiteit en kneedbaarheid gaven, waardoor de toepassingsmogelijkheden van deze stof werden uitgebreid. Rond 1950 werd PVC op industriële schaal gebruikt. Momenteel is PVC een van de meest gebruikte thermoplasten ter wereld.
Door Ana Luiza Lorenzen Lima
Scheikundeleraar
Heb je ooit gehoord van het chemische element chloor? Klik hier en leer over de kenmerken, eigenschappen, verkrijging, toepassingen en geschiedenis.
Ken de chemische samenstelling, productiebronnen en toepassingen van veel organische verbindingen, zoals onder andere aceton, alcohol en ether.
Lees meer over de eigenschappen, typen, nomenclatuur en waar koolwaterstoffen te vinden zijn.
Maak kennis met de chemische samenstelling van PVC-polymeer (polyvinylchloride), dat veel wordt gebruikt bij de productie van buizen en synthetische leermaterialen.
