reacties met basische oxiden zijn chemische verschijnselen waarbij een stof van deze klasse van oxiden in dezelfde container wordt geplaatst als een anorganisch zuur, een zuur oxide of een amfoteer oxide.
Zie ook:Reacties met amfotere oxiden
anorganisch zout en water zijn veelvoorkomende producten in een reactie met basische oxiden. Om erachter te komen of er anorganisch zout of water wordt geproduceerd, moeten we kijken naar de stof die het basische oxide in het reagens vergezelt. Bekijk de voorbeelden hieronder en begrijp hoe dit proces plaatsvindt.
Reacties met basische oxiden en anorganische zuren
Bij reacties tussen basische oxiden en anorganische zuren wordt een anorganisch zout en water gevormd, omdat het basische oxide-kation (Y+) interageert met het anion (X-) van het zuur en het hydroniumkation (H+) van het zuur interageert met het anion van het oxide:
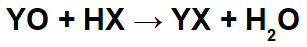
Voorbeeld: Radiumoxide en waterstofbromide
In deze reactie hebben we radiumoxide (RaO) en waterstofbromide (Hbr) als reactanten. Zo treden de volgende interacties op:
Radiokation (Ra+2) met het bromide-anion (Br-1) vormt het radiumbromidezout (RaBr2).
Hydronium kation (H+1) met het oxide-anion (O-2) water vormend (H2O).
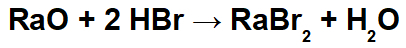
Zie ook:Reacties met dubbele oxiden
Reacties met basische oxiden en zure oxiden
Bij deze reacties wordt een anorganisch zout gevormd door de interactie tussen het basische oxide-kation (Y+) en het resulterende zuuranion (WODe-) van de chemische reactie tussen een zuuroxide en water.
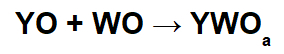
Voorbeeld: Natriumoxide en zwaveldioxide
In deze reactie hebben we natriumoxide (Na2O) en zwaveldioxide (SO2). Het is opmerkelijk dat, in eerste instantie, wanneer het zuuroxide interageert met water, we de vorming van zwaveligzuur (H2ENKEL EN ALLEEN3):
Niet stoppen nu... Er is meer na de reclame ;)

Door de vorming van dit zuur is de interactie tussen het natriumkation (Na+1) van het basische oxide en het sulfietanion (SO3-2) van het zuur, waardoor het natriumsulfietzout (Na2ENKEL EN ALLEEN3):
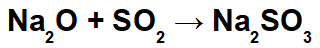
Reacties met basische oxiden en amfotere oxiden
Amfotere oxiden zijn stoffen die een dubbel chemisch gedrag vertonen: in aanwezigheid van een zure stof gedraagt het zich als een basisch oxide; in aanwezigheid van een stof met een basisch karakter gedraagt het zich als een zuuroxide.
Dus wanneer een basisch oxide reageert met een amfoteer oxide, zal dit zich gedragen als een zuuroxide en een anorganisch zuur vormen in aanwezigheid van water. De reactie tussen het anion van het anorganische zuur en het kation van het basische oxide zal een zoutproduct vormen.
Voorbeeld: Kaliumoxide en chroom III-oxide
In deze reactie hebben we kaliumoxide als reactanten (K2O) en chroomoxide (Cr2O3). Het is opmerkelijk dat, in eerste instantie, wanneer amfoteeroxide interageert met water, we de vorming van chromosomaal zuur (2HCrO2):

Door de vorming van dit zuur ontstaat de interactie tussen het kaliumkation (K+1) van het basische oxide en het chromietanion (SO3-2) van het zuur, waardoor het kaliumchromietzout (2KCrO2):

Door mij Diogo Lopes Dias
Wil je naar deze tekst verwijzen in een school- of academisch werk? Kijk:
DAGEN, Diogo Lopes. "Reacties met basische oxiden"; Braziliaanse School. Beschikbaar in: https://brasilescola.uol.com.br/quimica/reacoes-com-oxidos-basicos.htm. Betreden op 27 juli 2021.
Zoutnomenclatuur, zoutclassificatie, anionnaam, kationnaam, ijzersulfaat, ferrosulfaat, nitraat van zilver, kaliumchloride, natriumchloride, calciumchloride, zilvernitraat, kopersulfaat, carbonaat calcium.


