Bij oxidatiereacties met secundaire alcoholen zijn die waarin de interactie tussen een organische verbinding uit de groep van alcoholen, die secundair moet zijn, en het zogenaamde Bayer-reagens (KMnO4) in een zuur medium.
Wanneer het reagens van Bayer zich in een zuur medium bevindt (aq/H+), ondergaat het een ontledingsreactie, afkomstig van kaliumoxide, mangaanoxide II en ontluikende zuurstofatomen, zoals we kunnen zien in de volgende vergelijking:
2 kmnO4(aq/H+) → 2 MnO + K2O + 5 [O]
In elke oxidatiereactie, de ontluikende zuurstof, ontstaan door de ontleding van kaliumpermanganaat in een zuur milieu, de koolstofketens aanvallen die pi-bindingen hebben tussen koolstofatomen (alkenen, alkynen en alkadiënen) of die gesloten zijn (cyclanen, aromatische cycli), waardoor nieuwe chemische verbindingen ontstaan.
In het geval van oxidatiereactie in secundaire alcoholen, voordat u het reactiemechanisme begrijpt, moet u het concept van een secundaire alcohol onthouden. wordt genoemd secundaire alcohol
een waarin de hydroxyl (OH) is gekoppeld aan a secundaire koolstof (koolstof direct gebonden aan twee andere koolstofatomen). Zie de weergave van een secundaire alcohol: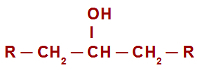
Algemene structuurformule van een secundaire alcohol
Bij elke oxidatiereactie in alcoholen vallen ontluikende zuurstofatomen de waterstofatomen aan die zich bevinden op de koolstof met de hydroxylgroep. In het geval van oxidatiereacties in secundaire alcoholen, hebben zuurstofatomen slechts één waterstofatoom om aan te vallen in elke structuur van dit type alcohol.
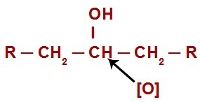
Ontluikende zuurstof die een secundaire alcohol aanvalt
Bij het aanvallen van de waterstof (H) die aanwezig is in de hydroxylkoolstof (OH), vormt de ontluikende zuurstof ([O]) een nieuwe hydroxylgroep op dezelfde koolstof. Dus we hebben een gemino diol in de gevangenis. Omdat geminodiol (HO – C – OH) onstabiel is, valt het uiteen in een watermolecuul.Tussen de koolstof en zuurstof die overblijft van een van de hydroxylen ontstaat echter een dubbele binding (pi en sigma).
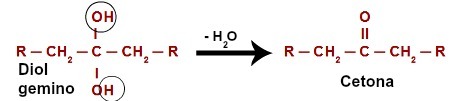
Chemische vergelijking van de oxidatie van een secundaire alcohol
Het product dat is ontstaan uit een oxidatiereactie van secundaire alcoholen is altijd een keton, want de dubbele binding wordt altijd gegenereerd aan de secundaire koolstof, wat resulteert in een carbonyl tussen twee koolstoffen, waardoor een keton wordt gevormd.
Zie nu een voorbeeld van de oxidatiereactie in secundaire alcoholen.
Voorbeeld: Butaan-2-ol
O butaan-2-ol is een secundaire alcohol, aangezien de hydroxyl is bevestigd aan een secundair koolstofatoom. Dus, op de koolstof die de hydroxyl heeft, is er maar één waterstof. We kunnen dit feit controleren in de onderstaande structuur:

Bij blootstelling aan een medium dat water, zuur en KMnO. bevat4 (reagens van Bayer), de je waterstof wordt aangevallen door een ontluikende zuurstof, transformeren in een nieuwe hydroxyl, wat resulteert in een gemino-diol.

Ten slotte is er een ontleding van de twee hydroxylen die aanwezig zijn in de geminodiol, wat resulteert in een watermolecuul en een keton, vanwege de noodzaak om een binding te creëren tussen koolstof en een van de zuurstofatomen van de afgebroken hydroxylen.

wij kunnen vertegenwoordigen de gehele butaan-2-ol oxidatiereactie door de volgende vergelijking:

Door mij Diogo Lopes Dias
Bron: Brazilië School - https://brasilescola.uol.com.br/quimica/reacoes-oxidacao-alcoois-secundarios.htm
