Aminozuren zijn organische moleculen die ten minste één aminogroep hebben - NH2 en een carboxylgroep - COOH in zijn structuur.
Aminozuren worden gebruikt bij de synthese van eiwitten, die naast enkele hormonen ook spieren, pezen, kraakbeen, bindweefsel, nagels en haar vormen. Zo binden ze zich aan elkaar om eiwitten te vormen, waardoor ze de "grondstof" zijn van deze macronutriënten.
Er zijn twee grote groepen aminozuren:
- Natuurlijke of niet-essentiële aminozuren: Dit zijn de aminozuren die door het lichaam zelf worden aangemaakt, 12 in totaal: glycine, alanine, serine, histidine, asparagine, glutamine, cysteïne, proline, tyrosine, arginine, asparaginezuur en zuur glutaminezuur;
- Essentiële aminozuren: Het zijn aminozuren die niet door het lichaam worden gesynthetiseerd en die via voedsel moeten worden verkregen. Ze komen overeen met acht aminozuren: fenylalanine, valine, tryptofaan, threonine, lysine, leucine, isoleucine en methionine.
Essentiële aminozuren komen voor in eiwitrijke voedingsmiddelen zoals vlees, vis, melk, eieren en peulvruchten (bonen, soja, linzen).
Samenstelling en structuur
Alle 20 bestaande aminozuren zijn α-aminozuren, dat wil zeggen dat de aminogroep en de carboxylgroep aan dezelfde koolstof (alfakoolstof) zijn bevestigd. Een aminozuur wordt gedefinieerd door zijn zijgroep (R).
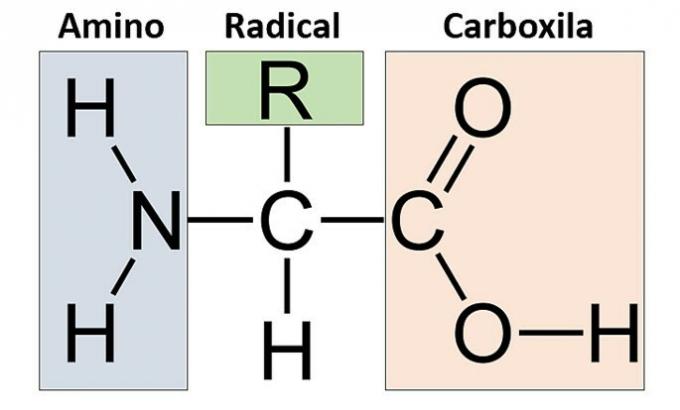
Alle aminozuren hebben dus een aminegroep gemeen (NH2) en een carboxyl- of zuurgroep (COOH) gebonden aan hetzelfde koolstofatoom, dat op zijn beurt gebonden is aan een waterstofatoom en aan een radicaal (R) dat varieert van het ene aminozuur tot het andere.
Vanwege het zure karakter van de carboxylgroep en het basische karakter van de aminogroep, wanneer aminozuren worden opgelost in water, lijden ze neutralisatie interne en worden dipolaire ionen, een elektrisch neutrale chemische verbinding.
Door deze eigenschap van aminozuren kunnen ze zowel met zuur als met base reageren. Verbindingen met dit gedrag worden amfoteren genoemd.
peptidebinding
De binding die de aminozuren verbindt, wordt een peptidebinding genoemd, gekenmerkt door de reactie van de aminegroep van het ene aminozuur met de carboxylgroep van een ander, met afgifte van een molecuul van water.
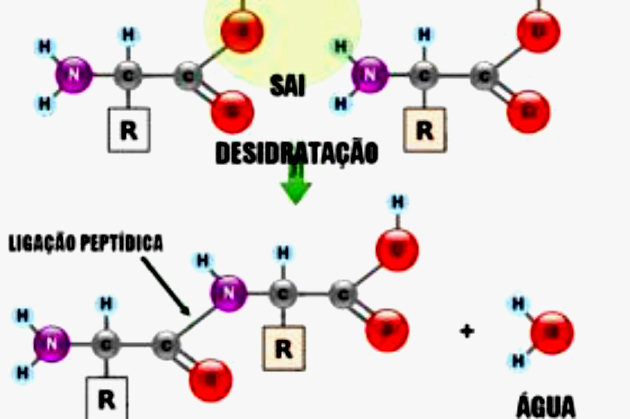
Twee aminozuren verbonden door een peptidebinding vormen een molecuul dat een dipeptide wordt genoemd. Verschillende aminozuren verbonden door verschillende peptidebindingen vormen een macromolecuul dat een polypeptide wordt genoemd.
Een eiwitmolecuul kan honderden aminozuren aan elkaar hebben. Hemoglobine is bijvoorbeeld opgebouwd uit 547 aminozuren.
Lees meer, lees ook:
- Peptiden en peptidebindingen
- Eiwitsynthese
- genetische code