O Fasen diagram is een grafiek waarmee u kunt bepalen in welke fysieke toestand een stof zich op een bepaald moment bevindt, waarbij u de temperatuur en druk kent.
Laboratoriummetingen worden gebruikt om het fasediagram van een bepaalde stof te bouwen.
Het diagram is verdeeld in drie gebieden, die de vaste, vloeibare en damptoestand vertegenwoordigen.
De stippen op de lijnen die deze gebieden afbakenen, geven de waarden van temperatuur en druk aan die de stof in twee toestanden kan hebben.
Een fasediagram heeft de volgende elementen:
- kromme van Fusie: scheidt de gebieden die overeenkomen met vaste en vloeibare toestanden.
- kromme van verdamping: scheidt de gebieden die overeenkomen met de vloeistof- en dampfase.
- kromme van sublimatie: scheidt de gebieden die overeenkomen met de vaste fase en de dampfase.
- drievoudig punt: snijpunt van de drie curven (fusie, verdamping en sublimatie). Dit punt geeft de temperatuur- en drukwaarden aan dat de stof tegelijkertijd in de drie toestanden kan zijn.
- Kritisch punt: geeft de hoogste temperatuur aan dat de stof damp is. Vanaf dat moment is het niet meer mogelijk om onderscheid te maken tussen vloeistof- en damptoestanden. Bij temperaturen boven het kritische punt wordt de stof een gas.
In de onderstaande figuur presenteren we een weergave van een fasediagram:

Lees meer bij: Veranderingen in fysieke toestand.
smeltcurve
Stoffen nemen in het algemeen in volume toe wanneer ze fusie ondergaan en nemen daarentegen in volume af wanneer ze stollen. Als gevolg hiervan leidt een verhoging van de druk tot een verhoging van het smeltpunt (smelttemperatuur).
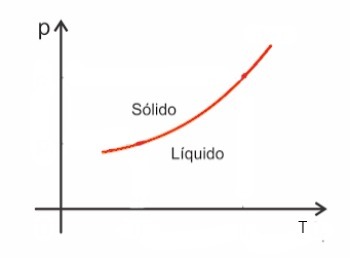
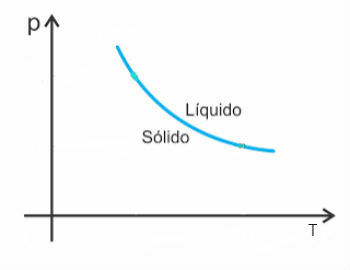
Er zijn echter enkele uitzonderingen, waaronder water, dat bij het smelten in volume afneemt. In dit geval veroorzaakt een verhoging van de druk een verlaging van het smeltpunt.
De smeltcurve van deze stoffen ziet er dus als volgt uit:
Voorbeeld
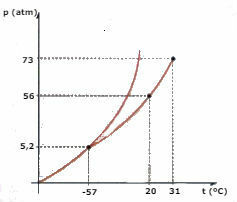
Overweeg het CO-fasediagram2 (kooldioxide) hieronder weergegeven en beantwoord de vragen:
a) Welke fase is de CO2 , wanneer de temperatuur -60 ºC is en de druk 50 atm is?
b) Een bepaalde hoeveelheid CO2 vloeistof wordt onderworpen aan een druk van 56 atm en wordt opgesloten in een container. Als de vloeistof wordt verwarmd en de druk constant wordt gehouden, wat is dan de temperatuurwaarde waarbij verdamping optreedt?
c) Wat is de temperatuur- en drukwaarde van het tripelpunt van CO2?
d) Een stuk droogijs (CO2) wordt onderworpen aan een druk van 2 atm. Het wordt verwarmd en handhaaft een constante druk. Op een bepaald moment begint er een faseverandering plaats te vinden. Wat is de naam van deze wijziging?
Resolutie:
a) Als we het diagram bekijken, concluderen we dat de CO2 zal in de vaste fase zijn.
b) Verdamping vindt plaats wanneer de temperatuur 20°C bereikt.
c) Het tripelpunt komt overeen met het snijpunt van de drie krommen, in het geval van CO2, wanneer het een temperatuur heeft van -57°C en een druk van 5,2 atm, kunnen de drie fysieke toestanden naast elkaar bestaan.
d) Sublimatie zal plaatsvinden
Lees voor meer informatie ook:
- stollen
- Smelt- en kookpunt
- Verdamping
- condensatie
Opgelost Oefeningen
1) Vijand - 2000
Zelfs vandaag de dag is het heel gewoon dat mensen aardewerken containers (potten of ongeglazuurde keramische potten) gebruiken om water te besparen op een temperatuur die lager is dan die van de omgeving. Dit is zo omdat:
a) klei isoleert water uit de omgeving en houdt het altijd op een lagere temperatuur dan zijn eigen, alsof het piepschuim is.
b) klei heeft de kracht om water te "bevriezen" vanwege zijn chemische samenstelling. Bij de reactie verliest water warmte.
c) de klei is poreus, waardoor er water doorheen kan. Een deel van dit water verdampt en neemt warmte op van de moringa en de rest van het water, dat vervolgens wordt afgekoeld.
d) de klei is poreus, waardoor water aan de buitenkant van de kan kan bezinken. Het buitenwater is altijd op een hogere temperatuur dan het binnenwater.
e) Moringa is een soort natuurlijke koelkast, die hygroscopische stoffen vrijgeeft die de temperatuur van het water op natuurlijke wijze verlagen.
Alternatief c: klei is poreus en laat water door. Een deel van dit water verdampt en neemt warmte op van de moringa en de rest van het water, dat vervolgens wordt afgekoeld.
2) Ita - 2013
Beschouw het hypothetische fasediagram schematisch weergegeven in de volgende afbeelding:

Waar staan de punten A, B, C, D en E voor?
punt A: sublimatiepunt
punt B: drievoudig punt
C-punt: smelt-/stolpunt
punt D: verdampings-/condensatiepunt
punt E: kritiek punt
3) UECE - 2009
Kijkend naar het onderstaande PT-fasediagram. Er kan terecht worden geconcludeerd dat een stof die het sublimatieproces heeft doorlopen het traject volgt:

a) X of Y
b) Y of U
c) U of V
d) T of X
Alternatief b: Y of U


