Nitratiereacties zijn substitutiereacties die plaatsvinden door salpeterzuur (HNO3). Dit type reactie treedt vooral op met alkanen en met benzeen en zijn derivaten, waarbij een van de waterstofatomen die aan de keten of aan de aromatische kern vastzitten, wordt vervangen door de NO-groep.2, waardoor een nitroverbinding en water ontstaan.
Zie enkele voorbeelden:
1. Nitratie van een alkaan:
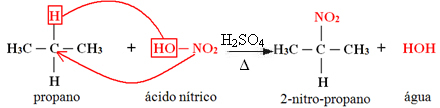
Wanneer het alkaan meer dan twee koolstofatomen heeft, wordt een mengsel van verschillende gesubstitueerde verbindingen gevormd. De hoeveelheid van elke verkregen verbinding zal evenredig zijn met de volgende volgorde van gemak waarmee waterstof in het molecuul wordt afgegeven:

In het bovenstaande geval is er geen tertiaire koolstof, er is slechts één secundaire en twee primaire; dus de grootste hoeveelheid verbinding die als een product wordt gevormd, zal 2-nitropropaan zijn.
Als er voldoende salpeterzuur is, kan een andere waterstof worden vervangen door de nitrogroep, waardoor 2-dinitropropaan ontstaat (structuur hieronder), een verbinding die veel wordt gebruikt als additief voor dieselolie, waardoor het octaangetal wordt verhoogd en de uitstoot van roet.
BIJ DE2
│
H3C─C─CH3
│
BIJ DE2
2. Benzeennitratie:
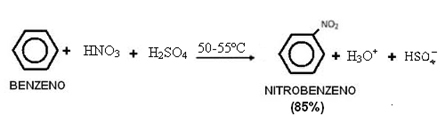
Merk op dat deze reactie plaatsvindt in aanwezigheid van warmte, aangezien de benzeen wordt verwarmd met een sulfonhydraatmengsel, dwz geconcentreerd salpeterzuur met geconcentreerd zwavelzuur. Zwavelzuur is een katalysator, waardoor de reactiesnelheid toeneemt omdat benzeen langzaam reageert met salpeterzuur.
3. Nitratie van benzeenderivaten:
In dergelijke gevallen zal de plaats van substitutie afhangen van de substituentgroep of functionele groep die aan de aromatische kern is bevestigd. de teksten "Stuurradicalen in de benzeenring" en "Elektronische effecten van meta- en ortho-naar-directors-radicalen” meer uitleg over hoe dit gebeurt.
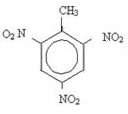
Aromatische ringen kunnen nitreren en aanleiding geven tot explosieven. Een voorbeeld is trinitrotolueen (2-methyl-1,3,5-trinitrobenzeen), beter bekend als TNT en er zijn verschillende pigmenten die voornamelijk in weefsels worden gebruikt.
Door Jennifer Fogaça
Afgestudeerd in scheikunde
Bron: Brazilië School - https://brasilescola.uol.com.br/quimica/reacoes-organicas-nitracao.htm
