U peptiden zijn biomoleculen gevormd door twee of meer aminozuren. De binding van peptiden vindt plaats via covalente chemische bindingen, genaamd, peptidebindingen. Enkele voorbeelden van peptiden zijn: glutathion, galanine, oxytocine, bradykinine, amanitine, thyrotrofine, cholecystokinine, vasopressine en enkefaline.
aminozuren
Allereerst is het de moeite waard eraan te denken dat de aminozuren zijn organische moleculen gevormd door een aminegroep - NH2 en een carboxylgroep - COOH, die worden beschouwd als de basiseenheden van peptiden en eiwitten.
Zo vormt een reeks aminozuren de eiwitten die bij hun synthese worden gebruikt. Ze worden ingedeeld in natuurlijke en essentiële aminozuren, waarbij de eerste door het lichaam zelf wordt gesynthetiseerd en de andere aminozuren die in de natuur worden gevonden, dat wil zeggen in voedsel.
Eiwitten
Bij eiwitten het zijn macromoleculen gevormd door de keten van aminozuren. Het zijn uiterst belangrijke verbindingen voor het goed functioneren van het lichaam, in wezen gevormd uit koolstof, waterstof, stikstof en zuurstof.
Op die manier worden peptiden als kleine eiwitten beschouwd, dat wil zeggen dat het fragmenten van eiwitten zijn en daarom worden ze gevormd door kleinere aantallen aminozuren in verhouding tot eiwitten.
Weet ook over de Eiwitstructuur.
Functies van peptiden
Net als eiwitten zijn peptiden chemische verbindingen die verschillende essentiële functies voor het leven aanduiden, namelijk:
- Reguleert de activiteit van meerdere systemen
- Hulp bij DNA-synthese
- Aminozuurtransport
- Metabolisme van drugs en giftige stoffen
- celregeneratie
- Ontstekingsremmend effect
- Stimulatie of remming van eetlust
- Stimuleert de urineproductie
- Reguleert hormonale en neurotransmitteractiviteit
- immuunfunctie
- natuurlijke antibiotica
Peptide Link
Peptidebindingen zijn covalente chemische bindingen (moleculaire bindingen) die optreden tussen twee of meer peptiden, door de reactie tussen een carbonzuur (-COOH) en een aminegroep (-NH2), waardoor een watermolecuul vrijkomt (H2O) in een proces dat uitdrogingssynthese wordt genoemd. Zo verenigt een waterstof (H) afkomstig van de aminegroep zich met een hydroxyl (-OH) van de carboxylgroep, waardoor het watermolecuul wordt gevormd.
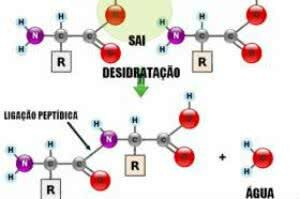 Peptide Link
Peptide Link
Aan de andere kant, om een peptidebinding te verbreken of ongedaan te maken, volstaat het om een watermolecuul toe te voegen dat het tegenovergestelde proces van uitdroging zal plaatsvinden, hydrolyse genaamd.
Het is de moeite waard om te onthouden dat peptiden biomoleculen zijn die worden gevormd door twee of meer aminozuren en dat de vereniging van veel peptiden eiwitten vormt. Samengevat vormen de peptidebindingen eiwitten, essentieel voor het goed functioneren van het lichaam.
Nomenclatuur
Afhankelijk van het aantal aminozuren dat in het molecuul aanwezig is, worden de peptiden ingedeeld in:
- Dipeptide: gevormd door twee aminozuren
- tripeptide: gevormd door drie aminozuren
- tetrapeptide: gevormd door vier aminozuren
- oligopeptide: van 4 tot 50 aminozuren
- Polypeptide: opgebouwd uit meer dan 50 aminozuren