DE distillatie het is een van de processen van scheiding van homogene mengsels die plaatsvindt door koken, waarbij de vloeistof wordt verdampt en vervolgens wordt gecondenseerd. De mengsels die worden gescheiden, hebben dus verschillende kookpunten.
Met andere woorden, destillatie is een fysisch-chemisch proces van scheiding van mengsels dat plaatsvindt door verwarming en koeling van de mengsels. Bij verhitting van het mengsel wordt eerst de stof met het laagste kookpunt, dat wil zeggen de meest vluchtige, verdampt.
Destillatie wordt uitgevoerd in chemische laboratoria en industrieën met behulp van specifieke apparatuur (condensor, thermometer, distillatie, bunsensproeier, beker, verwarmingsmantel, fractioneringskolom), bijvoorbeeld bij het scheiden van water van alcohol of water van de zout.
Een natuurlijk voorbeeld van het distillatieproces is te zien wanneer waterdruppels condenseren op koudere dagen. Bovendien worden de zogenaamde gedistilleerde dranken (cachaça, wodka, cognac, tequila, rum, whisky) geproduceerd via het fractionele distillatieproces, dat al sinds de oudheid wordt gebruikt.
Soorten distillatie
Destillatie kan op twee manieren plaatsvinden, afhankelijk van de aard van de afzonderlijke mengsels:
Eenvoudige distillatie
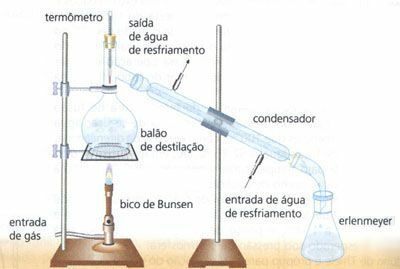 Eenvoudige distillatie
Eenvoudige distillatie
Scheiding van een homogeen mengsel van vast en vloeibaar, bijv. water (H2O) van het zout (NaCl). Op deze manier wordt het water verdampt door middel van verwarming, die door de condensor gaat in de vorm van vloeistof (waterdruppels), waar het zout wordt vastgehouden en gescheiden in een container genaamd a distillatie.
Gefractioneerde destillatie
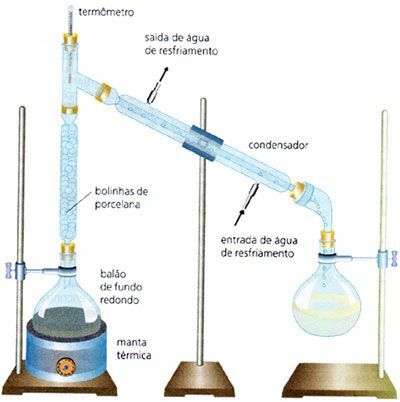 Gefractioneerde destillatie
Gefractioneerde destillatie
Op grote schaal gebruikt in de industrie, is het de scheiding van een homogeen mengsel van vloeistof en vloeistof, door bijvoorbeeld water en alcohol (het kookpunt van water is 100°C en het kookpunt van ethylalcohol) is 78°C). Het wordt uitgevoerd door mengsels met zeer nauwe kookpunten. In tegenstelling tot het eenvoudige destillatieproces is er in dit geval een fractioneringskolom.
Oliedestillatie
Voor het verkrijgen van aardolieproducten (benzine, kerosine, stookolie, paraffine, asfalt), het distillatieproces gefractioneerd wordt gebruikt waarbij de vloeistof met het laagste kookpunt eerst wordt gescheiden totdat de vloeistof met het hoogste kookpunt wordt bereikt. kokend.
onthoud dat de Aardolie het is een natuurlijke stof die bestaat uit verschillende organische componenten, met name koolwaterstoffen (koolstof- en waterstofmoleculen).
azeotrope distillatie
Azeotrope destillatie vindt plaats wanneer de scheiding van mengsels een azeotroop vormt, dat wil zeggen, ze hebben een lage vluchtigheid en punt constante kookpunten, die niet kunnen worden gescheiden door de eenvoudige methode van destillatie, bijv. zoutzuur (HCL) en water (H2O).
Leuke weetjes: wist je dat?
Gedestilleerd water (gedemineraliseerd water) is een zuivere stof die wordt verkregen door destillatie en wordt over het algemeen gebruikt in het laboratorium. Merk op dat het water dat we drinken niet zuiver is, dat wil zeggen dat het minerale zouten bevat. Gedestilleerd water kan echter zowel voor menselijke consumptie als voor de behandeling van bepaalde ziekten worden gebruikt, bijvoorbeeld nierstenen.
Vul je onderzoek aan door de artikelen te lezen:
- Smelt- en kookpunt
- Liquefactie of condensatie
- Verdamping
- Scheiding van mengsels
Controleer toelatingsexamenvragen met commentaar becommentarieerd: oefeningen over het mengen van scheiding.


