In de tekst "geometrische isomeer of cis-trans” werd getoond hoe geometrische ruimtelijke isomerie of cis-trans. In het kort, de isomeer cis komt overeen met verbindingen waarvan de gelijke liganden op elk koolstofatoom in hetzelfde vlak liggen; al in de isomeer trans, ze staan aan weerszijden.
Dit wordt geïdentificeerd door de oorsprong van deze termen, die uit het Latijn komt, waar cis betekent "naast" en trans "aan de overkant".
Deze nomenclatuur is erg handig wanneer twee koolstoffen elk slechts twee verschillende liganden hebben. Deze termen kunnen echter dubbelzinnig zijn wanneer wordt verwezen naar alkenen, waarvan de koolstofatomen met dubbele binding meer dan twee verschillende liganden in de set hebben.
Beschouw bijvoorbeeld de onderstaande verbinding:

Merk op dat op koolstof X het laagste atoomnummer ligand is CH3, en op koolstof ja is de H Maar als we stellen dat deze verbinding de isomeer is, cis, zou de volgende vraag kunnen rijzen: hoe is zij cis als de verbindingsgroepen gelijk zijn (CH3) aan weerszijden staan?
Om deze dubbelzinnigheid te vermijden, is het daarom correcter om in deze gevallen de nomenclatuur E-Z te gebruiken, waar de letter E van het Duitse woord komt engen, wat "tegengestelden" betekent en Z komt van het Duitse woord zusammen, wat 'samen' betekent. Deze nomenclatuur volgt de volgende regel:

Als we deze prioriteitsregel toepassen op 2-chloorbu-2-een, hebben we dat in koolstof X het ligand met het hoogste atoomnummer is Cl, en op koolstof ja is de CH3. We hebben dus de volgende isomeren:
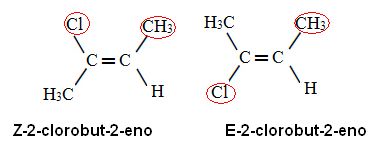
In het eerste geval bevinden de liganden met de hoogste atoomnummers zich aan dezelfde kant van het vlak (Z) en in het tweede geval bevinden ze zich aan weerszijden (E).
Dit komt ook voor bij cyclische verbindingen. Het is belangrijk om te onthouden dat het niet correct is om de termen cis en Z, en trans en E, met elkaar in verband te brengen, aangezien het verschillende naamgevingssystemen zijn.
Door Jennifer Fogaça
Afgestudeerd in scheikunde
Bron: Brazilië School - https://brasilescola.uol.com.br/quimica/isomeria-e-z-no-lugar-cis-trans.htm

