Bij hydratatie reacties in alkadiënen zij zijn toevoeging reacties, dat wil zeggen, de componenten (hydronium en hydroxide) van het watermolecuul worden toegevoegd aan een alkadieen.
U alkadiënen zijn koolwaterstoffen met een open keten en twee dubbele bindingen (gevormd door een sigma en een pi) tussen koolstofatomen, zoals we kunnen zien in de volgende structuur:

Structuurformule van een alkadieen
voor de hydratatiereactie in alkadiënen wordt uitgevoerd, is het essentieel dat de pi-binding, aanwezig in de dubbele binding, wordt verbroken door de invloed van warmte en zwavelzuur (H2ENKEL EN ALLEEN4). Met het verbreken van de pi-binding verschijnen twee bindingsplaatsen, elk op een van de koolstoffen die bij de dubbele binding betrokken zijn.

Opkomst van bindingsplaatsen met verstoring van pi-binding
Het verschijnen van bindingsplaatsen op het alkadieenmolecuul is noodzakelijk voor de ionen (H+ en oh-) uit het water worden toegevoegd aan het alkadieen, waarbij bijvoorbeeld een dialcohol (alcohol met twee hydroxylen).
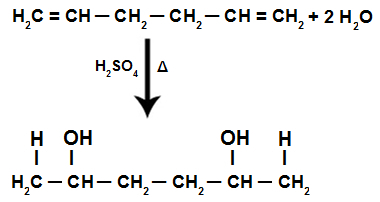
Toevoeging van H+ en oh- in de structuur van een alkadieen
OPMERKING: De toevoeging van de H+ en oh- in de alkadieenstructuur volgt de Regel van Markovnikov, dat wil zeggen de H+ bindt aan de meest gehydrogeneerde koolstof, en de OH- bindt aan de minder gehydrogeneerde koolstof.

Voorbeeld van de toepassing van de Markovnikov-regel bij de hydratatie van alkadiënen
Omdat er verschillende soorten alkadiënen zijn met betrekking tot de positie van de dubbele bindingen, kan het zijn dat de hydratatie van een alkadieen verschillende verbindingen vormt. Zie de volgende gevallen:
→ Geaccumuleerde of gecondenseerde alkadieen
Het is een alkadieen dat tegelijkertijd twee dubbele bindingen heeft met drie atomen van koolstof, dat wil zeggen, er is geen enkele binding die de koolstoffen scheidt die bij de bindingen betrokken zijn verdubbelt.

Structuurformule van een geaccumuleerde alkadieen
Tijdens de hydratatiereactie van een afwisselend alkadieen worden de pi-bindingen verbroken, zijnde de H+ toegevoegd aan de meer gehydrogeneerde koolstoffen en de OH- toegevoegd aan minder gehydrogeneerde koolstoffen:
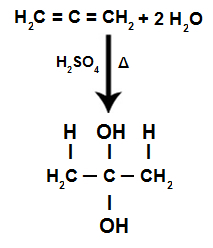
Geaccumuleerde alkadieenhydratatiereactievergelijking
We hebben dat bij de hydratatie van een opgehoopt alkadieen, hetzelfde koolstofatoom de twee hydroxylen ontvangt, waardoor een tweelingalcohol wordt gevormd, wat een onstabiele structuur is.

Structuur van de tweeling gevormde alcohol
Omdat de tweelingalcohol onstabiel is, hebben we de vorming van een watermolecuul met de componenten van de twee hydroxylen en de vorming van een pi-binding tussen koolstof en zuurstof.
Niet stoppen nu... Er is meer na de reclame ;)

Vorming van een keton uit een tweelingalcohol
Daarom zal de hydratatiereactie van geaccumuleerde alkadiënen resulteren in de vorming van a keton.
→ Geconjugeerd of alternatief alkadieen
Het is een alkadieen dat twee dubbele bindingen heeft waarbij tegelijkertijd vier koolstofatomen, dat wil zeggen, er is een enkele binding die de koolstofatomen scheidt die bij de bindingen betrokken zijn verdubbelt.
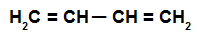
Structuurformule van een afwisselend alkadieen
Bij afwisselende alkadiënen treedt de resonantie van hun dubbele bindingen op. Dus de elektronen van de pi-binding veranderen van positie (rode pijlen), zoals in het volgende diagram:
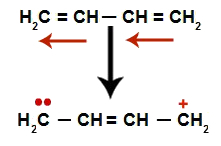
Schematische weergave van de resonantie in een afwisselend alkadieen
We hebben over het algemeen het uiterlijk van een dubbele binding precies tussen de koolstoffen waar de twee dubbele bindingen eerder waren en het creëren van twee bindingsplaatsen, één op elke koolstof die niet langer de dubbele binding maakt (in het voorbeeld koolstof 1 en 4). Koolstof 1 en 4 van de keten krijgen de H+ en de oh- uit het water.

Gedeeltelijke hydratatie in afwisselend alkadieen
Na resonantie wordt de pi-binding van de nieuwe dubbele binding verbroken en een H+ en een oh- worden toegevoegd aan het alkadieenmolecuul. De OH wordt toegevoegd aan de koolstof die zich het dichtst bij de eerste toegevoegde OH-groep bevindt, omdat deze de elektronische aantrekking van de groep ondergaat, die meer elektronegatief is.

Beëindiging van hydratatie in een afwisselend alkadieen
Vanwege de resonantie zeggen we dat het afwisselende alkadieen een 1,4-hydratatie onderging, waarbij een dialcohol werd gevormd.
→ Alkadieen geïsoleerd
Het is een alkadieen dat twee dubbele bindingen heeft met minstens vijf atomen tegelijk. van koolstof, dat wil zeggen, er zijn ten minste twee enkele bindingen die de koolstoffen scheiden die bij de bindingen betrokken zijn. verdubbelt.

Structuurformule van een geïsoleerd alkadieen
Tijdens de hydratatiereactie van een geïsoleerd alkadieen worden de pi-bindingen verbroken, de H+ toegevoegd aan de meer gehydrogeneerde koolstoffen en de OH- toegevoegd aan de minder gehydrogeneerde koolstoffen.

Geïsoleerde alkadieenhydratatiereactievergelijking
Daarom hebben we bij de toevoeging van een geïsoleerd alkadieen alleen de vorming van een diaalcohol.
Door mij Diogo Lopes Dias
Wil je naar deze tekst verwijzen in een school- of academisch werk? Kijken:
DAGEN, Diogo Lopes. "Hydratatiereacties in alkadiënen"; Brazilië School. Beschikbaar in: https://brasilescola.uol.com.br/quimica/reacoes-hidratacao-alcadienos.htm. Betreden op 28 juni 2021.

