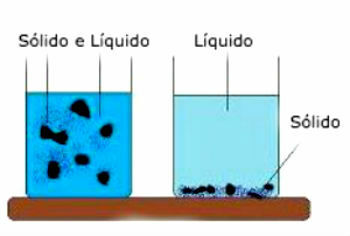
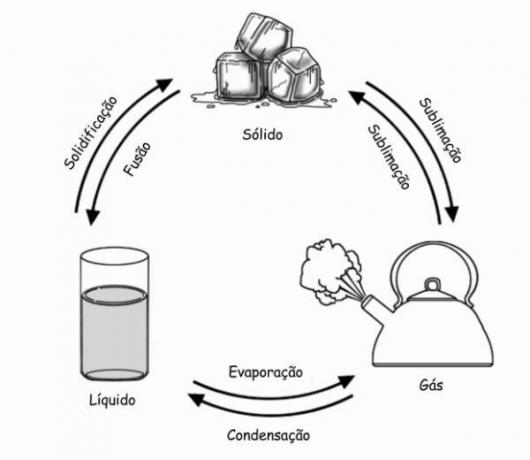
DE oorsprong van Periodiek systeem vond plaats in het begin van de 19e eeuw, rond 1829, toen scheikundigen destijds besloten om manieren voor te stellen om de chemische elementen tot dan bekend.
Aan het begin van de 19e eeuw hadden scheikundigen kennis over verschillende kenmerken (dichtheid, atoommassa, reactiviteit, smeltpunt, kookpunt, fysische toestand) van dertig chemische elementen. Deze kennis diende als uitgangspunt voor de oorsprong van het periodiek systeem.
Meer dan 200 jaar lang probeerden verschillende scheikundigen manieren voor te stellen om de chemische elementen te organiseren, dat wil zeggen de Het periodiek systeem dat we vandaag kennen, had eigenlijk verschillende oorsprongen, zoals door de geschiedenis heen veel pogingen waren uitgevoerd.
Mindmap: oorsprong van het periodiek systeem
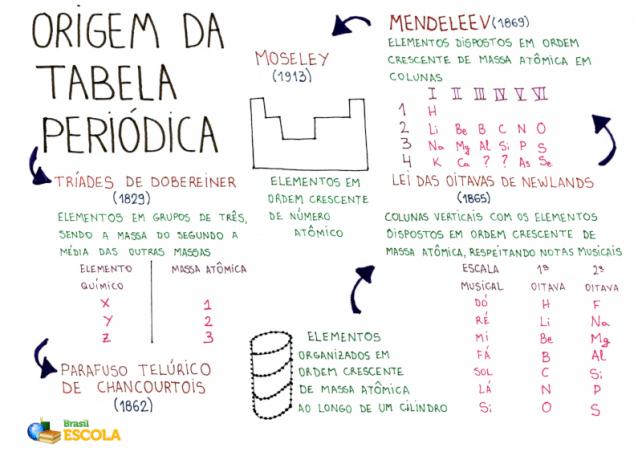
*Om deze mindmap te downloaden, Klik hier!
Hier zijn enkele van de chemici die hebben uitgeblonken in het proberen de elementen in een tabel te ordenen.
Dobereiner Triads

Illustratie door Johann Wolfgang Dobereiner *
In het jaar 1829 organiseerde de Duitse chemicus Johann Wolfgang Dobereiner het eerste periodiek systeem in de geschiedenis. Het bevatte de dertig chemische elementen die tot dan toe bekend waren en werd door hem de Dobereiner-triaden genoemd.
DE Dobereiner periodiek systeem het werd een triade genoemd omdat de elementen in groepen van 3 waren georganiseerd. Elke groep had elementen met vergelijkbare chemische kenmerken.
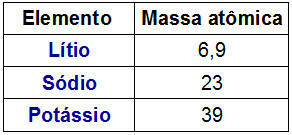
Vertegenwoordiging van een Dobereiner-triade
Een interessant feit over Dobereiner-drieklanken is dat de atoom massa van het centrale element van de triade was precies het resultaat van het rekenkundig gemiddelde tussen de atoommassa's van de andere twee elementen van de triade.

Tellurische schroef van Alexandre de Chancourtois
In het jaar 1862 schreef de Franse geoloog en mineraloog Alexandre de Chancourtois hij besloot een organisatie van de destijds bekende chemische elementen voor te stellen om hun toepassing in de mineralogie te vergemakkelijken. DE Chancourtois tafel het heette tellurische schroef.

Vertegenwoordiging van de Chancourtois tellurische schroefis
Chancourtois verdeelde de chemische elementen (donkere vlekken in de afbeelding) in oplopende volgorde van atomaire massa langs een spiraalvormige band die in een cilinder bestaat. Met deze organisatie merkte Chancourtois op dat elementen die op dezelfde verticale lijn waren geplaatst vergelijkbare chemische eigenschappen hadden.
Wet van Octaven
Niet stoppen nu... Er is meer na de reclame ;)
Wet van octaven was de naam die de Engelse chemicus J.A.R. Nieuwe landen, in het jaar 1865, naar het periodiek systeem. Omdat Newlands ook muzikant is, dekte hij de tafel volgens de muzieknoten (do, there, re, mi, fa, sol, there, si).
Newlands organiseerde de 61 chemische elementen die destijds bekend waren in oplopende volgorde van atomaire massa en plaatste ze in verticale kolommen. Elk van de verticale kolommen had zeven elementen.
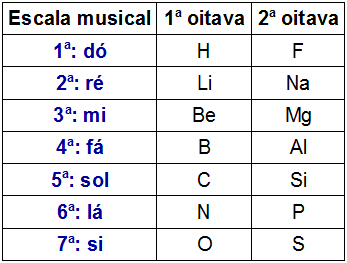
Twee octaven vertegenwoordiging van Newlands
Newlands merkte op dat chemische elementen die aanwezig zijn in dezelfde horizontale lijn van verschillende octaven vergelijkbare chemische eigenschappen hadden. Het eerste element van een octaaf had dus vergelijkbare eigenschappen als het eerste element van het andere octaaf, enzovoort.
Het periodiek systeem van Mendelejev

Illustratie door de chemicus Mendelejev **
Mendelejev, tijdens zijn werk met de chemische elementen, had hij de gewoonte om de eigenschappen van elk van hen op kaarten te schrijven. Op een gegeven moment, in het jaar 1869, besloot hij deze fiches in oplopende volgorde van atoommassa te plaatsen.
Direct nadat hij de elementen in oplopende volgorde van atomaire massa had gerangschikt, behield Mendelejev het patroon, maar plaatste de elementen in horizontale en verticale kolommen, met respect voor de kenmerken en overeenkomsten van de elementen.
Moseley Periodiek Systeem
In het jaar 1913 schreef de Engelse scheikundige HenryMoseley, gebaseerd op de tabel voorgesteld door Mendelejev, stelde het periodiek systeem samen in de patronen die we vandaag kennen.
In tegenstelling tot Mendelejev rangschikte Moseley de elementen in oplopende volgorde van atoomnummer, hield de organisatie in horizontale en verticale kolommen, maar plaatste de elementen met dezelfde chemische eigenschappen in dezelfde verticale kolommen.
huidige periodiek systeem
Na 1913 onderging het door Moseley voorgestelde periodiek systeem geen grote veranderingen, in feite onderging het enkele updates, omdat er enkele chemische elementen werden ontdekt.
In vergelijking met de huidige tabel toonde de Moseley-tabel bijvoorbeeld niet de chemische elementen met atoomnummers tussen 110 en 118. Ook bevond de actinidereeks zich boven de lanthanidereeks.
DE laatste update uitgevoerd in het periodiek systeem was in 2016, toen de elementen 113, 115, 117 en 118 er officieel onderdeel van werden.
* Afbeelding tegoed: Yangchao/ rolluik. inclusief
** Afbeelding tegoed: Olga Popova/ rolluik. inclusief
Door mij Diogo Lopes Dias