dissociatie van basissen het is een fysiek proces die optreedt bij deze belangrijke groep anorganische stoffen wanneer ze worden opgelost in water, of wanneer ze door het fusieproces gaan (doorgang van de vaste toestand naar de vloeibare toestand via) verwarming).
In het algemeen is het fenomeen van basis dissociatie het is het vrijkomen van de kationen en anionen die de vormen Ionische verbinding, die in dit geval de basis is. Dus tijdens de basis dissociatie, het uitkomen van ionen die al in de verbinding bestaan, dat wil zeggen dat er geen nieuwe ionen worden gevormd.
De base wordt gevormd door een metaal (X), dat het kation van de verbinding is, of door het ammoniumkation (NH-groep4+), gebonden aan het hydroxide-anion (weergegeven door de OH-groep), zoals in de onderstaande afbeeldingen:
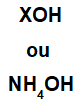
Algemene weergaven van een basisformule
de vorm van vertegenwoordigen de basis dissociatie het wordt gedaan door een vergelijking waarin we in de reactant de base hebben en in de producten de ionen (kationen en anionen). Wat het verschil maakt, is hoe de dissociatie plaatsvindt:
Oplossen van de base in water:
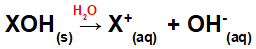
Vergelijking die de dissociatie van een base in een waterig medium weergeeft
Dissociatie door basisfusie:
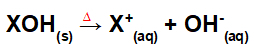
Vergelijking die de dissociatie van een base door het fusieproces weergeeft
Door de algemene vergelijkingen hierboven te analyseren, verifiëren we dat we in al deze vergelijkingen altijd de base, het kation (dat is de metaal- of NH-groep4+) en het anion (OH-). Maar zijn ze allemaal zo? Zit er geen verschil tussen? Op de eerste vraag is het antwoord nee en op de tweede vraag is het antwoord ja.
Niet stoppen nu... Er is meer na de reclame ;)
Wanneer we de dissociatie van een basis, is het van fundamenteel belang om eerst de basisformule te analyseren, omdat we daaruit de belasting van de kunnen bepalen kation en de molhoeveelheid hydroxide-anionen, aangezien de molhoeveelheid kation standaard is (altijd 1 mol).
Het is de moeite waard eraan te denken dat de hoeveelheid OH-groepen in de baseformule de lading van het kation en de hoeveelheid in mol van het hydroxide-anion bij de dissociatie van de base bepaalt.
Laten we eens kijken naar de voorbeelden van aluminiumhydroxide [Al(OH)3] en goudhydroxide (AuOH). In de aluminiumbasisformule zijn er drie OH-groepen en in de goudbasisformule slechts één OH-groep. Dus bij de dissociatie van deze basen hebben we:
Al (OH) dissociatie3:
Aangezien deze base drie OH-groepen in de formule heeft, zal de lading op het kation +3 zijn en is de hoeveelheid in mol anionen gelijk aan 3 mol, zoals we kunnen zien in de volgende vergelijking:
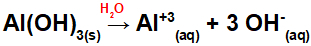
Dissociatievergelijking op basis van aluminium in waterig medium
Dissociatie van AuOH:
Omdat deze base een OH-groep in de formule heeft, zal de lading op het kation +1 zijn en is de hoeveelheid in mol anionen gelijk aan 1 mol, zoals we kunnen zien in de volgende vergelijking:
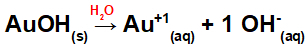
Vergelijking van basedissociatie met goud in waterig medium
Door mij Diogo Lopes Dias
Wil je naar deze tekst verwijzen in een school- of academisch werk? Kijken:
DAGEN, Diogo Lopes. "Wat is basisdissociatie?"; Brazilië School. Beschikbaar in: https://brasilescola.uol.com.br/o-que-e/quimica/o-que-e-dissociacao-das-bases.htm. Betreden op 27 juni 2021.
Chemie

Dissociatie en ionisatie, Italiaanse wetenschapper Volta, elektrische stroom, Zweedse fysisch chemicus Svant August Arrhenius, theorie van Arrhenius, positieve ionen, kationen, negatieve ionen, anionen, bijtende soda, keukenzout, polaire moleculen, dissociatie ionisch,