Over het algemeen is de pure substanties komen nauwelijks geïsoleerd in de natuur voor, ze worden gevonden in de vorm van mengsels, dat wil zeggen, geassocieerd met andere stoffen. Dit betekent dat wij en bijna alles om ons heen voorbeelden zijn van mengsels van de meest uiteenlopende zuivere stoffen.
In deze tekst zullen we leren wat het is en wat de classificaties van zuivere stoffen en mengsels zijn.
pure substanties
pure substanties zijn materialen met een chemische samenstelling en eigendommen constante fysische en chemische, omdat ze niet veranderen bij constante druk en temperatuur.
Over het algemeen kunnen zuivere stoffen op twee manieren worden ingedeeld:
a) Eenvoudige stoffen
Het zijn chemische verbindingen gevormd door atomen van hetzelfde chemische element. Bijvoorbeeld:
→ H2 (Hydrogen gas)
Waterstofgasmoleculen worden gevormd door twee atomen van het scheikundige element waterstof, dus het is een eenvoudige stof.
→ O3 (Ozongas)
Ozongasmoleculen worden gevormd door drie atomen van het chemische element Zuurstof, dus het is een eenvoudige stof.
Er is ook de mogelijkheid dat atomen van hetzelfde chemische element totaal verschillende eenvoudige stoffen vormen, de allotropen. Een voorbeeld van allotropie dit is het geval van het scheikundige element Zuurstof, dat de gasstoffen zuurstof vormt (O2) en ozongas (O3).
Niet stoppen nu... Er is meer na de reclame ;)
B) samengestelde stoffen
Het zijn chemische verbindingen gevormd door atomen van verschillende chemische elementen. Voorbeelden:
→ CO2 (Koolgas of Kooldioxide)
Kooldioxidemoleculen worden gevormd door één atoom van het element koolstof en twee atomen van het element zuurstof. Omdat de chemische elementen verschillend zijn, is het een samengestelde stof.
→ kmnO4 (Kaliumpermanganaat)
O ionenformule van kaliumpermanganaat wordt gevormd door één atoom van het element kalium, één atoom van het element mangaan en vier atomen van het element zuurstof.
Mindmap: pure stof en mengsel

* Om de mindmap in PDF te downloaden, Klik hier!
mengsels
Mengen het is de vereniging van twee of meer verschillende stoffen (ongeacht of ze enkelvoudig of samengesteld zijn). Het heeft fysieke kenmerken (smeltpunt, kookpunt, dichtheid, taaiheid, enz.) die anders en variabel (niet vast) zijn in vergelijking met de stoffen waaruit het bestaat.
Een mengsel van water en natriumchloride heeft bijvoorbeeld een totaal ander smeltpunt dan het smeltpunt van water (0OC) en natriumchloride (803OC) alleen.
a) Homogene mengsels
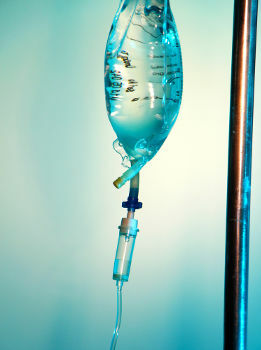
Zoutoplossing is een homogeen mengsel gevormd door water, glucose en natriumchloride
Homogene mengsels hebben slechts één fase (een enkele visuele verschijning). Ze worden gevormd wanneer een materiaal het vermogen heeft om een ander op te lossen. Voorbeelden:
water en natriumchloride;
water en glucose;
benzine en ethanol;
atmosferische lucht (zuurstofgas, stikstofgas, kooldioxide, waterdamp enz.);
azijnzuur en water;
aardolie (benzine, kerosine, smeerolie, enz.);
zoutoplossing.
b) Heterogene mengsels

Melk is een heterogeen mengsel omdat het een vloeibare fase (water) en een vaste fase (vet) heeft
Heterogene mengsels hebben meer dan één fase (twee of meer visuele aspecten). Ze worden gevormd wanneer het ene materiaal het andere niet oplost. Voorbeelden:
Graniet;
Melk;
Bloed;
Water en zand;
Water dit is Leeuw;
Water en benzine.
* Mindmap door Victor Ricardo Ferreira
Scheikundeleraar
Door mij Diogo Lopes Dias
Wil je naar deze tekst verwijzen in een school- of academisch werk? Kijken:
DAGEN, Diogo Lopes. "zuivere stoffen en mengsels"; Brazilië School. Beschikbaar in: https://brasilescola.uol.com.br/quimica/mistura-e-substancias-puras.htm. Betreden op 28 juni 2021.
Chemie

Zie de definitie van elementaire scheikundeconcepten zoals materie, energie, stof, mengsel, lichaam, object, massa, volume en systeem.

