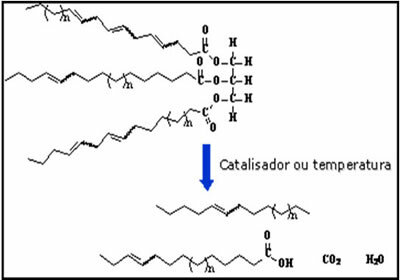
Net als de cyclanen, alkenen, alkynen, onder andere de alkadiënen heb ook last van de telefoontjes toevoeging reacties. In de tekst over reacties in diens, zult u zien dat de additiereacties afhankelijk zijn van het type dieen waaraan wordt gewerkt. De dienen kunnen grofweg worden ingedeeld in:
gecondenseerd of geaccumuleerd (geen enkele binding tussen de twee doubles);
Vb: H2C = CH-CH3
geconjugeerd of afgewisseld (slechts een enkele binding tussen de twee doubles);
Vb: H2C = CH—CH = CH2
geïsoleerd (ten minste twee enkele bindingen tussen de twee dubbele).
Vb: H2C = CH-CH2—CH2—CH = CH2
De Diels-Alder-reactie werd in 1928 ontwikkeld door twee Duitse chemici, Otto Paul Hermann Diels en Kurt Alder. Dit is een zeer belangrijke reactie binnen de organische chemie omdat het mogelijk maakt:
dieenkoolwaterstoffen identificeren;
verkrijg verzadigde cyclische koolwaterstoffen (bij voorkeur cyclohexanen).
Deze organische reactie vindt alleen plaats in alkadienen of geconjugeerde of afgewisselde diënen en heet
toevoeging 1.4. De verbinding waarin we de toevoeging van 1,4 op een eenvoudigere manier kunnen waarnemen, is maar-1,3-dieen, zoals hieronder weergegeven:H2C = CH—CH = CH2
OPMERKING: In deze verbinding hebben we het voorkomen van resonantie fenomeen, waarin de elektronen van de twee pi-bindingen door de keten bewegen. Een paar pi elektronen electron begint het centrale deel van de keten te bezetten (tussen koolstof 2 en 3), terwijl de elektronen van de andere pi-binding worden verschoven naar een van de eindkoolstofatomen. We hebben dus bindingsplaatsen op koolstof 1 en 4 en een dubbel tussen koolstof 2 en 3.

Resonantie in de maar-2,3-dieenstructuur
Niet stoppen nu... Er is meer na de reclame ;)
Bij Diels-Alder-reactie, een van de reagentia is een geconjugeerd dieen, terwijl de andere een organische verbinding is die aanwezig kan zijn een telefoontje dubbel tussen koolstofatomen. Hieronder is een voorbeeld van een Diels-Alder-reactie tussen but-2,3-dieen en propeen:
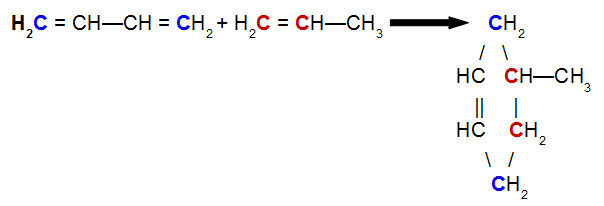
Vergelijking van een Diels-Alder-reactie van but-2,3-dieen met propeen
Als we de bovenstaande vergelijking analyseren, kunnen we zien dat koolstofatomen 1 en 4 (beide in blauw) van maar-2,3-dieenbinding respectievelijk tot koolstof 1 en 2 (beide rood) van propeen, waardoor een vertakt cyclene ontstaat, de 4-methylcyclohexeen. Dit komt door de resonantie in het but-2,3-dieenmolecuul, dat een pi-binding tussen koolstof 2 en 3 verschuift, en de breuk van de pi-binding tussen koolstoffen 1 en 2 van propeen.
OBS.²: Het is belangrijk om te benadrukken dat, ongeacht de verbinding die reageert met het geconjugeerde alkadieen, er alleen een breuk in de pi-binding tussen koolstofatomen in de keten zal zijn. Als de structuur pi-bindingen heeft tussen andere atomen dan koolstof, zullen ze niet worden verbroken. Hieronder is een voorbeeld van een structuur die kan reageren met a alkadieen in een Diels-Alder-reactie, wat resulteert in het verbreken van de pi-binding tussen de koolstofatomen (in blauw) van de dubbele binding.
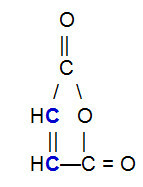
Structuurformule van maleïnezuuranhydride
Door mij Diogo Lopes Dias
Wil je naar deze tekst verwijzen in een school- of academisch werk? Kijken:
DAGEN, Diogo Lopes. "Diels-Alder-reacties"; Brazilië School. Beschikbaar in: https://brasilescola.uol.com.br/quimica/reacoes-diels-alder.htm. Betreden op 28 juni 2021.
Chemie

Alkenen, gas, etheen, ethyleen, kunststoffen, synthetisch rubber, kleurstoffen, synthetische stoffen, explosieven, kraken van aardolie, polyethyleen, olefiant gas, olefinen, koolwaterstoffen, ketting acyclische koolstofdioxide.