Organische verbindingen kunnen op verschillende manieren worden weergegeven, zoals een platte structuurformule, een vereenvoudigde of verkorte structuurformule of een streepjesformule. De eenvoudigste weergave is echter via de molecuulformule.

Laten we dus eens kijken hoe we de molecuulformule van organische verbindingen kunnen bepalen, op basis van de andere hierboven genoemde formules.
1. Door de platte structuurformule:deze formule toont de rangschikking of rangschikking van atomen in het molecuul. Hieronder staat bijvoorbeeld de platte structuurformule van een van de in benzine aanwezige koolwaterstoffen.

Merk op dat in deze formule alle atomen en alle bestaande bindingen daartussen worden weergegeven. Nu, om de molecuulformule van deze verbinding te bepalen, tel je het aantal atomen van elk element en plaats je een index rechtsonder op het betreffende element.
Een belangrijk aspect dat moet worden benadrukt, is dat: we beginnen de molecuulformule van organische verbindingen altijd met het element koolstof, aangezien het het hoofdbestanddeel van deze stoffen is. Zie het voorbeeld:
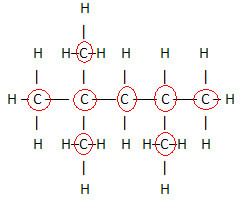
Aangezien er 8 koolstofatomen zijn, beginnen we de molecuulformule als volgt te schrijven: Ç8
Om deze formule te voltooien, tellen we de hoeveelheid waterstofatomen:
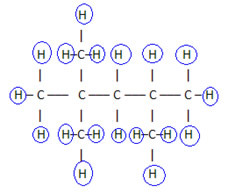
Dus jouw moleculaire formule é Ç8H18.
2. Door de vereenvoudigde of verkorte structuurformule: in dit type formule wordt de hoeveelheid waterstofatomen afgekort. Kijk bijvoorbeeld naar dezelfde formule voor het molecuul dat in benzine wordt gevonden, nu in een gecondenseerde vorm:
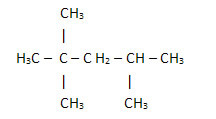
Niet stoppen nu... Er is meer na de reclame ;)
Op deze manier is het nog gemakkelijker om de hoeveelheid waterstofatomen te tellen, gewoon de indices (3 +3+ 3 +2 +1 +3 +3 = 18) bij elkaar optellen.
Maar laten we nu eens kijken naar de gecondenseerde structuurformule van linolzuur, die voorkomt in groenten zoals katoen, sojabonen, zonnebloemen, enz. en die wordt gebruikt in verven en vernissen:
H3C─CH2CH2CH2CH2CH═CH─CH2CH═CH─CH2CH2CH2CH2CH2CH2CH2COOH
Als we de hoeveelheid koolstoffen, waterstofatomen en zuurstofatomen tellen, hebben we het volgende: moleculaire formule van linolzuur: Ç18H32O2.
3. Via de slagformule: deze formule vereenvoudigt verder de weergave van organische verbindingen, omdat de groepen C, CH, CH. worden weggelaten2 en CH3.
Een voorbeeld is het linolzuurmolecuul, kijk hoe het eruit ziet:

Laten we eerst de hoeveelheid koolstofatomen tellen, onthoud dat in deze formule elke binding tussen koolstofatomen wordt weergegeven door het streepje. Dus de uiteinden, evenals de twee buigpunten, komen overeen met koolstofatomen.
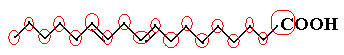
Dus we hebben: Ç18
Nu, om de hoeveelheid waterstofatomen te tellen, moeten we onthouden dat de bindingen tussen koolstoffen en waterstofatomen impliciet zijn, omdat bekend is dat koolstof vier bindingen maakt; dus het aantal bindingen dat ontbreekt, is de hoeveelheid waterstof die aan dat element is gebonden.
Zie onderstaande uitleg:
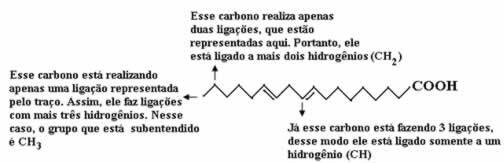
De hoeveelheid waterstof is dus: 32.

De hoeveelheid zuurstof is vrij eenvoudig te tellen, aangezien het er maar twee zijn. sinds de moleculaire formule é: Ç18H32O2.
Door Jennifer Fogaça
Afgestudeerd in scheikunde
Wil je naar deze tekst verwijzen in een school- of academisch werk? Kijken:
FOGAÇA, Jennifer Rocha Vargas. "Moleculaire formules van organische verbindingen"; Braziliaanse School. Beschikbaar in: https://brasilescola.uol.com.br/quimica/formulas-moleculares-compostos-organicos.htm. Betreden op 28 juni 2021.
Ruimtelijke formule van koolstof, elektronische formule van Lewis, vlakke structuur, elektronische paren, binding covalent, valentielaag, evolutie van het atoommodel, molecuulformule, structuurformule, formules driedimensionaal.
Chemische formules, platte structuurformule, Couper structuurformule, drievoudige binding, gas stikstof, elektronische formule, Lewis-formule, molecuulformule, enkele binding, dubbele binding, gas koolzuur.