Ze noemen zichzelf innerlijke overgangselementen alle 28 chemische elementen gelegen in de 6e en 7e periode van groep 3 (of familie IIIB) van de Periodiek systeem. Ze zijn meer specifiek buiten het hoofdgedeelte van de tabel geplaatst.
worden genoemd overgangselementen omdat ze niet tot families A behoren (representatieve elementen), maar ze kunnen niet worden verward met de elementen van externe overgang (elementen die tot families B behoren en in het hoofdgedeelte van de tabel zijn geplaatst) periodiek).
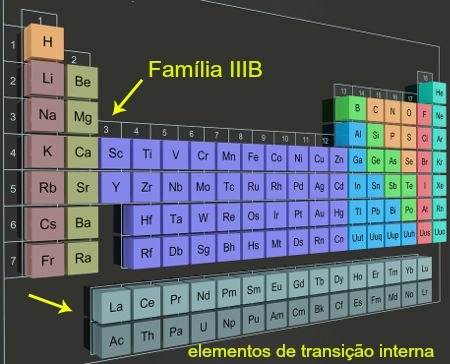
Interne overgangselementen in kolommen buiten het periodiek systeem
U innerlijke overgangselementen presenteren het f-subniveau als energieker. Een bewijs hiervan is dat elk van de horizontale kolommen die naar deze elementen verwijzen slechts 14 elementen heeft, waarbij 14 het maximale aantal is elektronen ondersteund door subniveau f.
a) Lanthanide-reeks
De lanthaniden zijn alle die uitsluitend behoren tot de 6e periode van de IIIB-familie, zo genoemd omdat het eerste element in de reeks lanthaan (La) is. Bekijk de namen en acroniemen van allemaal:
Lanthaan (La)
Cerium (C)
Praseodymium (pr)
Neodymium (Nd)
Promethium (pm)
Samarium (Sm)
Europium (ik)
Gadolinium (Gd)
Terbium (TB)
Dysprosium (Dy)
Holmium (Ho)
Erbium (Er)
Thulium (Tm)
Ytterbium (Yb)
Alle interne overgangselementen presenteren het 4f-subniveau als het meest energieke, dat wil zeggen, de elektronische distributie ze eindigen allemaal op dit subniveau, zoals we kunnen zien in de verdeling van twee elementen die tot de reeks behoren:
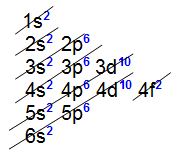
Elektronische distributie van het lanthanide-element Cerium

Elektronische distributie van het lanthanide-element Holmium
b) Actinide-reeks
Actiniden zijn alle die uitsluitend behoren tot de 7e periode van de IIIB-familie, zo genoemd omdat het eerste element in de reeks Actinium (Ac) is. Bekijk de namen en acroniemen van allemaal:
Actinium (Ac)
Thorium (D)
Protactinium (Pa)
uranium (U)
Neptunium (Np)
Plutonium (Pu)
Americium (Am)
Curium (cm)
Berkelium (Bk)
Californië (zie)
Einsteinium(n)
Fermium (Fm)
Mendelevium (MD)
Nobel (Nb)
Alle interne overgangselementen presenteren het 5f-subniveau als het meest energetische, dat wil zeggen de verdeling elektronica van allemaal eindigt op dit subniveau, zoals we kunnen zien in de verdeling van twee elementen die behoren tot de series:

Elektronische distributie van het uraniumactinide-element

Elektronische distributie van het actinide-element uit Californië
Door mij Diogo Lopes Dias
Bron: Brazilië School - https://brasilescola.uol.com.br/quimica/elementos-transicao-interna.htm
