Pārvietošanas reakcijas, ko sauc arī par aizstāšanas reakcijasvai joprojām no vienkārša apmaiņa, ir tie, kas rodas, kad vienkārša viela (ko veido viens elements) reaģē ar saliktu vielu, pēdējo “izspiežot” jaunā vienkāršā vielā.
Parasti mēs to varam definēt šādi:
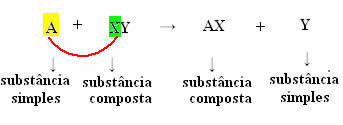
Bet, lai tas notiktu, vienkāršā viela, gadījumā, ko simbolizē A, jābūt reaktīvākam nekā elementam, kas tiks izspiests no savienojuma, pārveidojot sevi par jaunu vienkāršu vielu (Y).
Apskatīsim piemēru, kur notiek šī reakcija:
Ievērojiet zemāk esošo eksperimentu, kurā cinka loksni (Zn) ievieto vara sulfāta ūdens šķīdumā (CuSO4). Laika gaitā tiek atzīmēts, ka vara sulfāta šķīdums no zilas krāsas mainās uz mazāk intensīvu zilu, jo tas mainīja krāsu un uz cinka loksnes bija vara nogulsnes.

Mēs varam attēlot šo reakciju, izmantojot šādu ķīmisko vienādojumu:

Ņemiet vērā, ka cinks ir izspiests vara, kas nozīmē, ka cinks ir visreaktīvākais.
Tā kā abi ir metāli, mēs varam pārbaudīt, vai vienkārša apmaiņas reakcija notiks vai nē, analizējot metāla reaktivitātes rinda parādīts zemāk:
Nepārtrauciet tūlīt... Pēc reklāmas ir vairāk;)

Ņemiet vērā, ka varš faktiski ir mazāk reaktīvs nekā cinks, tādēļ, ja mēs nolēmām rīkoties pretēji iepriekšējam eksperimentam un ielieciet vara lokšņu cinka sulfāta šķīdumā, reakcija nenotiks, jo varš nespēs izspiest cinks.
Pārvietošanas reakcijas ir redoksreakcijas veids, jo notiek elektronu pāreja no vienkāršās vielas uz salikto. Iepriekš izskaidrotajā procesā cinks sākotnēji bija neitrālā formā, kas ir metāla, un kļuva par daļu no savienojuma, kurā tam ir 2+ lādiņš, tas ir, katrs cinka atoms ir zaudējis divus elektroni. Izmantojot varu, notiek pretējais, tas saņem divus elektronus, lai pārietu uz metālisko cietvielu.
Vienkāršas apmaiņas reakcijas gadījumā ar nemetāliem tiek uzskatīts: reakcija notiks tikai tad, ja visreaktīvākais nemetāls ir vienkāršā viela, kas var izspiest citu mazāk reaktīvu nemetālu. Ametālu reaktivitāte parādīta zemāk:

Autore Jennifer Fogaça
Beidzis ķīmiju
Vai vēlaties atsaukties uz šo tekstu skolas vai akadēmiskajā darbā? Skaties:
FOGAÇA, Jennifer Rocha Vargas. "Pārvietošana, aizstāšana vai vienkāršas apmaiņas reakcijas"; Brazīlijas skola. Pieejams: https://brasilescola.uol.com.br/quimica/reacoes-deslocamento-substituicao-ou-simples-troca.htm. Piekļuve 2021. gada 28. jūnijam.