Parasti reakcijas ūdens elektrolīze un magmatiskā elektrolīze tos veic ar grafīta un platīna elektrodiem, kas nepiedalās reakcijā; tie vada tikai elektrisko strāvu. Tomēr ir daži īpaši gadījumi, kad tas ir jāizmanto aktīvie elektrodi, tas ir, kas tiek reducēti un oksidēti.
Galvenie šo elektrodu izmantošanas gadījumi, kas piedalās redoksa procesā, ir šādi: a elektrolītiskā metāla attīrīšana, piemēram, cinks, kobalts, niķelis un galvenokārt varš; un arī galvanizācija. Apskatīsim, kā notiek katrs gadījums:
• Vara elektrolītiskā attīrīšana: šī elektrolītiskā vara attīrīšana var radīt aptuveni 99,9% tīrību, un to galvenokārt izmanto ražošanai vara vadi, kuriem, ja tiem ir vismazāk piemaisījumu, var būt spēja vadīt ļoti elektrisko strāvu samazināts.
Novērojiet, kā notiek šis process, redzot zemāk samontētās elektrolītiskās tvertnes shēmu:

Vara sulfāta ūdens šķīdumam (CuSo4 (aq)) - kas vada elektrību - tā, ka anods, kas ir nešķīsts metāla varš, zaudē elektronus, tas ir, tas oksidējas, atbrīvojot katjonus (Cu
2+), kas nogulsnējas uz negatīvās plāksnes. Tā var būt inerta platīna plāksne vai, labāk, tīra vara plāksne. Tas veido katodu, kas tiek reducēts, kad tajā tiek nogulsnēts varš. Tādējādi pusreakcijas, kas notiek elektrodos, ir:Nepārtrauciet tūlīt... Pēc reklāmas ir vairāk;)
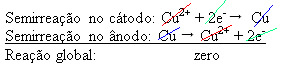
Fakts, ka tas deva nulles rezultātu, norāda, ka nebija ķīmiskas reakcijas, bet tikai vara transportēšana. Tvertnes apakšā ir citas nešķīstās vielas, kas bija varā, piemēram, zelts, sudrabs, silīcija dioksīds (smiltis) un citi minerāli, kurus pat var pārdot.
• Galvanizācija: materiālam, kas jāaizsargā no korozijas, tiek uzklāts metāla pārklājums.
Pārklājumam izvēlētais metāls, kas var būt hroms (hroms), niķelis (niķelis), sudrabs (sudrabs), zelts (apzeltījums) vai cinks (cinkošana) - būs anods, pozitīvais elektrods, kas tiek oksidēts, zaudējot elektronus. Tas tiek oksidēts aizsargātā materiāla vietā, jo tā reducēšanas potenciāls ir lielāks.
Negatīvais elektrods, tas ir, katods, kas uztver šos elektronus un notiek redukcija, ir pats materiāls, kas tika pārklāts. Tādā veidā tas paliek aizsargāts pat tad, ja tā virsma ir kaut kā pārkāpta.
Autore Jennifer Fogaça
Beidzis ķīmiju
Vai vēlaties atsaukties uz šo tekstu skolas vai akadēmiskajā darbā? Skaties:
FOGAÇA, Dženifera Roka Vargasa. "Elektrolīze ar aktīviem elektrodiem"; Brazīlijas skola. Pieejams: https://brasilescola.uol.com.br/quimica/eletrolise-com-eletrodos-ativos.htm. Piekļuve 2021. gada 28. jūnijam.
