Plkst organiskās pievienošanās reakcijas ir ļoti izplatītas un pētītas. Ir vērts atcerēties, ka tas ir reakcijas veids, kas kā galvenais un dominējošais mehānisms ir pārtraukt saiti vai saites, pi lai divi vai vairāki atomi varētu sākt būt ķēdes daļa.
Pievienošanas reakciju izmantošanas piemērs ir saistīts ar margarīna ražošana. Šis produkts, kas tik bieži sastopams cilvēku ikdienā, tiek veidots no esošo augu eļļu hidrogenēšanas (pievienošanas reakcijas) pi saites tās konstitūcijā.
Pievienošanas reakciju veidi ir:
hidrogenēšana (ūdeņraža atomu pievienošana);
Halogenēšana (halogēna atomu pievienošana: Cl2, br2, Es2 un F2);
Reakcija ar halogenīdu (pievienojot halogēnu saturošus neorganiskus ūdeņražus, piemēram, HCl, HI, Hbr un HF);
Hidratācija (hidronija pievienošana, H+un hidroksilgrupu, OH-).
Pievienošanas laikā līdz mitrināšana vai ar halogenīdu, The Markovņikova valdīšana mums ir ļoti svarīgi paredzēt veidojamos produktus. Šajā noteikumā mums ir tas atoms hidronijs (H+) neorganiskajam hidroksīdam vai ūdenim pievieno ūdeni
vairāk hidrogenēta oglekļa no dubultās saites. jau halogēns (Cl, Br, I, F) halogenīda vai hidroksilgrupa (OH-) ūdens pievienos mazāk hidrogenēta oglekļa no pi saites. Skatiet šī noteikuma piemērošanas piemēru šādā vienādojumā: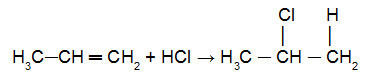
Proprēna reakcija ar HCl
Šajā vienādojumā mēs varam redzēt, ka (Cl) tika pievienots mazāk hidrogenētajam ogleklim pi saite, bet atoms hidronijs (H+) tika pievienots visvairāk hidrogenētajam oglekļa atomam pi saite.
ir tikai viens izņēmums uz Markovņikova likumu: Kharash reakcija. Tajā notiek inversija, tas ir, atoms hidronijs (H+) tiks pievienots grupai mazāk hidrogenēta oglekļa dod pi saite, tas ir halogēns (Br) halogenīda tiks pievienots vairāk hidrogenēta oglekļa dod pi saite. Sīkāk ir tas, ka šī reakcija notiek tikai vienā veidā:
Nepārtrauciet tūlīt... Pēc reklāmas ir vēl vairāk;)
Organiskā peroksīda klātbūtne;
Hbr. Izmantošana
PIEZĪME: ja šie nosacījumi nav izpildīti, Markovņikova valdīšana tiks izmantoti normāli.
Zemāk skatiet Kharash reakcija propilēnā:
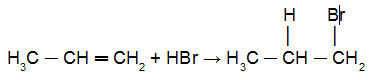
Propēna reakcija ar HBr peroksīda klātbūtnē
PIEZĪME: Ir vērts atzīmēt, ka organiskais peroksīds ir savienojums, kura sastāvā obligāti ir grupa (R─O─O─R). Kharash reakcijās visbiežāk izmantotais organiskais peroksīds tiek iegūts no karbonskābēm, un tam ir šāda struktūra:
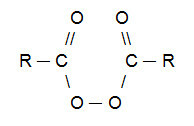
Organiskā peroksīda vispārējā strukturālā formula
Kharash reakcijas, lai apvērstu Markovņikova likumu, izskaidrojums ir tāds, ka sākotnēji peroksīds tiek sadalīts (1. solis), veidojot brīvos radikāļus ar diviem skābekļa atomiem, kas uzbrūk HBr ūdeņradim (2. darbība). Šī iemesla dēļ, kurš sākotnēji uzbruks alkēna molekulai, tas būs Br (3. darbība). Tikai pēc tam, kad ūdeņradis saistīsies ar alkēna ķēdi. Ievērojiet faktu secību:
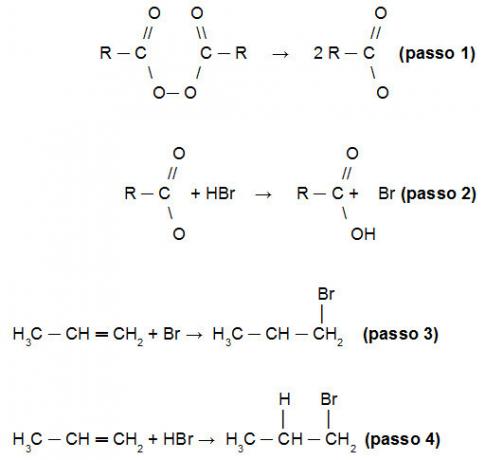
Kharash reakcijas mehānisma demonstrēšana
Autors: Diogo Lopes Dias
Vai vēlaties atsaukties uz šo tekstu skolas vai akadēmiskajā darbā? Skaties:
DIENAS, Diogo Lopes. "Kharash reakcija"; Brazīlijas skola. Pieejams: https://brasilescola.uol.com.br/quimica/reacao-kharash.htm. Piekļuve 2021. gada 28. jūnijam.

