Tekstā "Smadzeņu elektrolīze”, Tika paskaidrots, ka šis process notiek, kad elektriskā strāva tiek izvadīta izkausētā vielā (šķidrā stāvoklī) bez ūdens, un šādā veidā katjons saņem elektronus, un anjons ziedo elektronus tā, lai abiem elektriskais lādiņš būtu vienāds ar nulli un enerģiju uzkrājies.
Lai labāk saprastu, kā notiek magmatiskā elektrolīze, ņemsim vērā vienu no vissvarīgākajiem šāda veida procesa piemēriem, nātrija hlorīda vai galda sāls (NaCl) elektrolīzi.
Nātrija hlorīds dabā veidojas, elektronu pārnesot no nātrija (Na) uz hloru (Cl), kā norādīts zemāk:
2Na (s) + 1Cl2(g) → 2NaCl (s)

Šis process ir spontāns, bet šīs reakcijas apgrieztais process nav spontāns, tas ir, hlora gāzes (Cl2(g) - attēls zemāk) un metāliskais nātrijs (Na (s)) dabā nenotiek. Ja mēs vēlamies, lai tas notiktu, mums būs jāsāk process.
To var izdarīt ar magmatisko elektrolīzi. Sāls tiek uzkarsēts līdz temperatūrai virs 800,4 ° C, kas ir tā kušanas temperatūra; un tādā veidā tas saplūst, pārejot no cietas uz šķidru. Šajā fiziskajā stāvoklī jūsu Na joni+ un Cl- ir bez maksas.
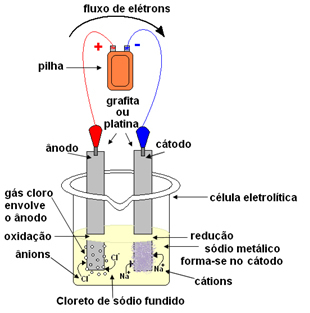
Pēc tam izkausēto sāli ievieto traukā, elektrolītiskajā traukā un divus inertu platīna vai grafīta elektrodus iemērc nātrija hlorīdā. Šie elektrodi ir savienoti ar avotu, kas rada tiešu elektrisko strāvu, piemēram, akumulatoru vai elementu.
Ar elektriskās strāvas pāreju notiek šādi:
- Baterijas vai šūnas negatīvais pols piegādā elektronus vienam no elektrodiem, kas kļūst par katodu;
- Katods: saņem elektronus no šūnas un kļūst par negatīvo polu, piesaistot Na katjonus+, jo pretējas maksas piesaista. Šie joni saņem elektronus no elektroda (katoda), un notiek to reducēšanās, veidojot metāla nātriju:
Samazinājums:Plkst+(ℓ) + un- → Ins)
Metāla nātrijs tiek nogulsnēts elektroda augšpusē un tiek nosūtīts uz rezervuāru.
- Anods: kļūst pozitīvi uzlādēts, piesaistot Cl anjonus- (tāpēc to sauc par anodu). Šie joni, nonākot saskarē ar anodu, zaudē savus elektronus, un tāpēc tie oksidējas, veidojot hlora atomus, kas uzreiz pa diviem apvienojas, veidojot hlora gāzi:
Oksidēšana:2Cl-(ℓ) → 2 un- + 1Cl2g)
Šī gāze burbuļo ap anodu, un to savāc sistēmai pielāgota stikla caurule.
Tādējādi vispārējo reakciju, kas notiek šajā gadījumā, sniedz:
Katods: 2Na+(ℓ) + 2e- → 2Nas)
Anods: 2Cl-(ℓ) → 2 un- + 1Cl2g) ____________
Globālā reakcija: 2Na+(ℓ) + 2Cl-(ℓ) → 2Nas) + 1Cl2g)
Vēl viens svarīgs aspekts, kas jāzina un kas tika uzsvērts minētā teksta beigās (magmatiskā elektrolīze), ir tas, ka elektrolīzei šūnai vai akumulatoram, ko izmanto elektriskās strāvas ģenerēšanai, ddp (potenciāla starpībai) jābūt vienādai vai lielākai par reakcija.
Apskatīsim to nātrija hlorīda elektrolīzes gadījumā, kuru mēs apsveram. Lai uzzinātu šīs reakcijas iespējamo atšķirību, pietiek ar katoda standarta reducēšanas potenciāla samazināšanu par anoda samazinājumu. Tas ir izskaidrots tekstā. Potenciāla akumulatora atšķirība .
Caur standarta samazināšanas potenciālu tabulu (E0sarkanā krāsā), mēs zinām, ka:
Plkst+(ℓ) + un- → Ins) UN0sarkans = -2,71
2Cl-(ℓ) → 2 un- + 1Cl2g) UN0sarkans = +1,36
Tagad vienkārši samaziniet šīs vērtības, lai uzzinātu globālās reakcijas iespējamo atšķirību:
∆Un0 = UN0sarkans (katods) - UN0sarkans (anods)
∆Un0 = -2,71 – (+ 1,36)
∆Un0 = - 4,07 V
Tāpēc tas nozīmē, ka izmantojamās šūnas vai akumulatora spriegumam jābūt vienādam vai lielākam par 4,07 V, lai veiktu nātrija hlorīda magmatisko elektrolīzi.
Negatīvā vērtība tikai norāda, ka tas nav spontāns process.. Bateriju gadījumā, kas ir spontāns process, elektromotora spēka vērtība (∆E0) vienmēr dod pozitīvu.
Autore Jennifer Fogaça
Beidzis ķīmiju
Avots: Brazīlijas skola - https://brasilescola.uol.com.br/quimica/eletrolise-Ignea-cloreto-sodio.htm
