Entropija tas ir sistēmas traucējumu pakāpes rādītājs, kas mēra enerģijas nepieejamību.
Tas ir fizisks daudzums, kas ir saistīts ar Otrais termodinamikas likums un ka tam ir tendence dabiski pieaugt Visumā.
Entropijas definīcija
“Traucējumi” nav jāsaprot kā “haoss”, bet gan kā sistēmas organizācijas veids.
Entropijas jēdziens dažreiz tiek pielietots citās zināšanu jomās ar šo traucējumu izjūtu, kas ir tuvāk veselajam saprātam.
Piemēram, iedomāsimies trīs burkas, viena ar mazām zilām bumbiņām, otra ar tāda paša veida bumbiņām, bet sarkana, bet trešā tukša.
Mēs paņemam tukšo katlu un zem tā liekam visas zilās bumbiņas un pa virsu visas sarkanās bumbiņas. Šajā gadījumā bumbiņas tiek atdalītas un sakārtotas pēc krāsas.
Kratot katlu, bumbiņas sāka sajaukt tā, ka noteiktā brīdī vairs nav sākotnējās atdalīšanas.
Pat ja mēs turpinām kratīt katlu, maz ticams, ka bumbiņas atgriezīsies tajā pašā sākotnējā organizācijā. Tas ir, sakārtotā sistēma (bumbiņas atdalītas ar krāsu) ir kļuvusi par nesakārtotu sistēmu (jauktas bumbiņas).

Tādējādi dabiska tendence ir palielināt sistēmas traucējumus, kas nozīmē entropijas palielināšanos. Tad mēs varam teikt, ka sistēmās: ΔS> 0, kur S ir entropija.
Arī saprast, kas tas ir entalpija.
Entropija un termodinamika
Entropijas koncepciju sāka izstrādāt franču inženieris un pētnieks Nikolass Sadijs Karnots.
Pētījumos par mehāniskās enerģijas pārveidošanu siltumā un otrādi viņš atklāja, ka nav iespējams izveidot pilnīgi efektīvu termisko mašīnu.
Pirmais termodinamikas likums būtībā nosaka, ka "enerģija tiek saglabāta". Tas nozīmē, ka fiziskajos procesos enerģija netiek zaudēta, tā tiek pārveidota no viena veida uz otru.
Piemēram, mašīna izmanto enerģiju, lai veiktu darbu, un šajā procesā mašīna uzsilst. Tas ir, mehāniskā enerģija tiek sadalīta siltuma enerģijā.
Siltuma enerģija vairs nemainās mehāniskā enerģija (ja tas notiktu, mašīna nekad nedarbotos), tāpēc process ir neatgriezenisks.
Vēlāk lords Kelvins papildināja Karnot pētījumu par termodinamisko procesu neatgriezeniskumu, radot pamatu Otrais termodinamikas likums.
Rūdolfs Klausiuss pirmais lietoja terminu Entropija 1865. gadā. Entropija būtu lieluma mērs Siltumenerģija kuru noteiktā temperatūrā nevar pārveidot par mehānisko enerģiju (nevar paveikt darbu).
Klausiuss izstrādāja matemātisko formulu pašlaik izmantotajai entropijas () S variācijai.
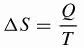
Būt,
ΔS: entropijas variācija (J / K)
J: siltuma pārnese (J)
T: temperatūra (K)
Lasīt arī:
- Termodinamika
- Carnot cikls
- Enerģija
- Enerģijas veidi
- Fizikas formulas
Atrisināti vingrinājumi
1) Enem - 2016. gads
Līdz 1824. gadam tika uzskatīts, ka siltuma dzinējiem, kuru piemēri ir tvaika dzinēji un pašreizējie iekšdedzes dzinēji, varētu būt ideāla darbība. Sadi Carnot parādīja, ka nav iespējams, ka 100% efektivitāte būtu siltuma mašīnai, kas darbojas ciklos starp diviem termiskiem avotiem (vienu karstu un otru aukstu). Šādi ierobežojumi rodas tāpēc, ka šīs mašīnas
a) veic mehānisku darbu.
b) radīt paaugstinātu entropiju.
c) izmantot adiabātiskās transformācijas.
d) ir pretrunā ar enerģijas saglabāšanas likumu.
e) darbojas tajā pašā temperatūrā kā karstais avots.
Alternatīva: b) radīt palielinātu entropiju.
2) Enem - 2011. gads
Motors var strādāt tikai tad, ja tas saņem enerģijas daudzumu no citas sistēmas. Šajā gadījumā degvielā uzkrāto enerģiju degšanas laikā daļēji atbrīvo, lai ierīce varētu darboties. Kad motors darbojas, daļu no enerģijas, kas pārveidota vai pārveidota degšanas laikā, nevar izmantot darba veikšanai. Tas nozīmē, ka pastāv enerģijas noplūde citā formā. Karvalju, A. X. Z.
Termiskā fizika. Belo Horizonte: Pax, 2009 (pielāgots).
Saskaņā ar tekstu enerģijas pārveidošanās, kas notiek motora darbības laikā, ir saistīta ar a
a) nav iespējams atbrīvot siltumu motora iekšpusē.
b) motora veiktais darbs nav kontrolējams.
c) nav iespējams pilnībā pārveidot siltumu par darbu.
d) siltuma enerģijas pārveidošana kinētikā nav iespējama.
e) degvielas potenciālā enerģijas izmantošana nav kontrolējama.
Alternatīva: c) nav iespējams pilnībā pārveidot siltumu par darbu.
Skatiet arī: Vingrinājumi par termodinamiku



