Tā kā ir tūkstošiem organisko savienojumu, izomērijas parādībai var būt vairākas formas. Tāpēc izomēriju pamatā var iedalīt divos veidos: plakans vai konstitucionāls izomērijs un kosmosa izomērisms vai stereoizomerisms. Katru minēto tipu var sadalīt sīkāk, kā parādīts šajā diagrammā:
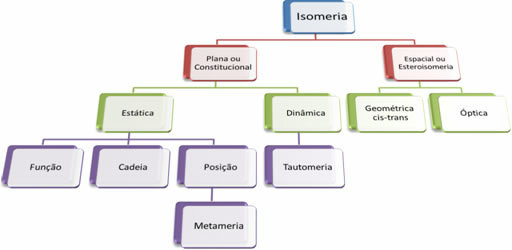
Skatīt katru gadījumu:
1. Plakans vai konstitucionāls izomērijs: Šāda veida izomēriem ir tāda pati molekulārā formula un tie atšķiras ar plakanām strukturālām formulām. Ir pieci plakanas izomērijas gadījumi: funkcija, ķēde, pozīcija, metamerisms un tautomerisms.
1.1.Funkcionāls vai funkcionāls izomērijs: Atšķirība starp izomēriem ir funkcionālajā grupā.
Piemērs: Molekulārā formula C3H6O
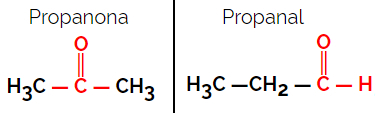
Ņemiet vērā, ka propanons ir no ketonu grupas un propanāls ir no aldehīdu grupas.
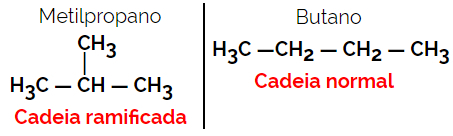
1.2. Ķēdes vai skeleta izomēri: Atšķirība starp izomēriem ir ķēdes tipā. Piemēram, viens izomērs ir atvērta ķēde un otra slēgta ķēde, vai viens ir normālas un otras sazarotas ķēdes, vai viens ir homogēna ķēde, bet otra ir neviendabīga.
Piemērs: Molekulārā formula C4H10
1.3.Pozicionālais vai pozicionālais izomērijs: Atšķirība ir nepiesātinājuma, funkcionālās grupas, heteroatomu vai aizstājēja stāvoklī.
Piemērs: Molekulārā formula C4H6

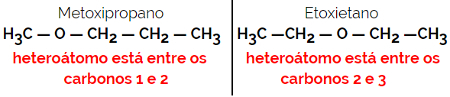
1.4.Kompensācijas izomērija vai metamērija: Tas ir īpašs stāvokļa izomērijas veids, kur atšķirība ir heteroatomu pozīcija.
Piemērs: Molekulārā formula C4H10O
1.5.Dinamiskā izomērija vai tautomērija: Tas ir īpašs funkcijas izomērijas veids, kurā izomēri pastāv līdzās dinamiskā līdzsvara šķīdumā. Divi galvenie tautomērijas veidi ir starp ketonu un enolu (ketoenola bilance) un starp aldehīdu un enolu (aldoenola līdzsvars).
Piemērs: Molekulārā formula C3H6O
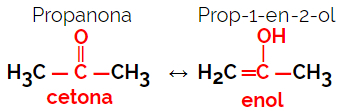
2. Kosmosa izomērisms vai steroizomerisms: Šajā gadījumā atšķirību starp izomēriem var vizualizēt tikai ar to atomu orientāciju telpā. Ir divu veidu stereoizomerisms: ģeometriskais izomērs un optiskais izomērijs.
2.1.Ģeometriskie vai cis-trans izomēri: Atšķirība ir tā, ka izomēru sauc par cis tam ir tie paši oglekļa ligandi dubultā saite vai cikliskie savienojumi plaknes vienā pusē. Izomēru ligandi tulk atrodas pretējās pusēs.
Piemērs: Molekulārā formula C2H2Cl2

Šos savienojumus sauc stereoizomēri.
2.2.Optiskais izomērs: Rodas, kad izomēri spēj novirzīt polarizētas gaismas staru. Ja tas saliek polarizēto gaismas staru pa kreisi, tas ir levorotārais izomērs, bet, ja tas liecas pa labi, to sauc par labās puses izomēru.
Piemērs:
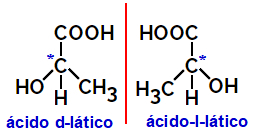
Tādas asimetriskas molekulas kā iepriekš redzamās, kas ir viena otras spoguļattēli un nav uzlikamas, sauc par enantiomēri.
Autore Jennifer Fogaça
Beidzis ķīmiju
Avots: Brazīlijas skola - https://brasilescola.uol.com.br/quimica/tipos-isomeria.htm