Jūs esteri ir skābekli saturoši organiskie savienojumi, kas veidojas ķīmiskā reakcijā starp a karbonskābe tas ir alkohols. Uzrāda funkcionālo grupu (sastāv no diviem skābekļa atomiem un diviem radikāļi R), kas attēlots zemāk:
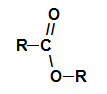
Estera vispārējā funkcionālā grupa
Strukturāli tas, kas raksturo esteris tā ir dažu alkilgrupu klātbūtne, kas pievienota tieši skābekļa atomam. Šajā gadījumā radikāls (R), kas pievienots ogleklim - kas, savukārt, ir divkārši piesaistīts skābeklim, var būt vai nu alkilgrupa, vai ūdeņraža atoms.
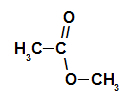
Estera ogļūdeņraža ķēde
esterifikācijas reakcija
runa ir par ķīmiskā reakcija, kuras rezultātā karboksilskābes un jebkura spirta mijiedarbībā rodas esteris un ūdens molekula, kā zemāk norādītajā vienādojumā:
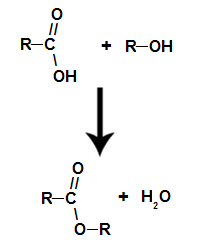
Ķīmiskais vienādojums, kas apzīmē estera veidošanos
Esterifikācijas laikā spirta hidroksilgrupa (OH) mijiedarbojas ar ūdeņradis (H) jonizējams no skābes hidroksila un veido ūdens molekula.
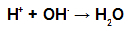
Ūdens molekulu veidojošās grupas esterifikācijā
jau esteris tas veidojas, savienojot spirta radikāļu (R) ar skābekli, kas pēc ūdens veidošanās paliek pāri skābes hidroksilam.
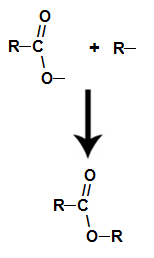
Estera molekulas veidošanās
Esteru raksturojums
Galvenās fizikālās īpašības, ko uzrāda esteri:
Viņiem ir augļu un ziedu aromāti;
zemie esteri molārā masa tie ir šķidri istabas temperatūrā, un tie, kuriem ir liela molārā masa, ir cieti;
Salīdzinot ar spirtiem un karbonskābēm, esteriem ir zemākas kušanas un viršanas temperatūras;
Salīdzinot ar ūdeni, zemākas molārās masas esteri ir mazāk blīvi;
Zemākās molārās masas esteri ir polāri, bet augstākās - nepolāri;
Polārajos esteros pārsvarā ir spēki pastāvīgs dipols; nepolārā dominē spēki izraisīts dipols;
Esteri ar mazāku molāro masu ūdenī šķīst slikti, un tie, kuru masa ir lielāka, ūdenī nešķīst.
Estera nosaukšanas kārtība
Pirms lietojat nosaukuma noteikuma a esteris, ir svarīgi atcerēties, ka šo savienojumu veido divu daļu savienojums, no kuriem viens nāk karbonskābes (sarkanā krāsā) un otra spirta (zilā krāsā), kā parādīts attēlā a sekot:
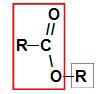
Esteru radošo daļu identifikācija
Saskaņā ar Starptautiskās tīrās un lietišķās ķīmijas savienības datiem (IUPAC), oficiālais noteikums par estera nosaukšanu ir:
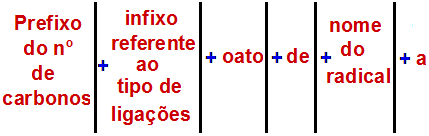
Estera nosaukšanas kārtība
Piezīme: Prefikss un uzraksts vienmēr atbilst karbonskābes daļai, un radikāļdaļa atbilst spirta daļai.
Tālāk skatiet dažus nosaukumu estera piemērošanas piemērus:
1. piemērs: aveņu esence
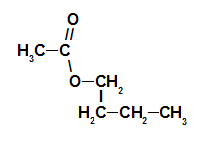
Aveņu esences estera strukturālā formula
Lai nosauktu šo esteri, mēs izmantojam:
Nē. PrefikssO ogļu: et, jo veidojošajai skābei ir divi ogļūdeņraži;
Infix par saišu veidu: an, jo veidojošajai skābei starp ogļām ir tikai atsevišķas saites;
rīcība;
iekšā;
Radikāls: butils, par to, ka secīgi ir četri ogļi;
The.
Tādējādi aveņu esencei atbilstošā estera nosaukums ir butiletanoāts.
2. piemērs: priežu čiekuru esence
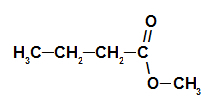
Priežu konusa estera strukturālā formula
Lai izveidotu šī estera nosaukumu, mēs izmantojam:
Nē. PrefikssO ogļu: bet, tā kā skābes veidošanā ir četri ogļūdeņraži;
Infix par saišu veidu: an, jo veidojošajai skābei starp ogļām ir tikai atsevišķas saites;
rīcība;
iekšā;
Radikāls: metilgrupa, jo veidojošajā alkoholā ir tikai viens ogleklis;
The.
Tādējādi priežu čiekuru esencei atbilstošā estera nosaukums ir metilbutanoāts.
3. piemērs: zemeņu esence
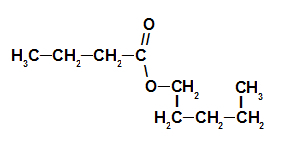
Zemeņu esences estera strukturālā formula
Lai nosauktu šo esteri, mēs izmantojam:
Nē. PrefikssO ogļu: bet, jo veidojošajā skābē ir četri ogļūdeņraži;
Infix par saišu veidu: an, jo veidojošajai skābei starp ogļām ir tikai atsevišķas saites;
rīcība;
iekšā;
Radikāls: pentils, jo veidojošajam alkoholam ir pieci ogļi pēc kārtas;
The.
Tādējādi esteru nosaukums, kas atbilst zemeņu esencei, ir pentilbutanoāts.
Esteru izmantošana
Esteri ir plaši pazīstami ar lietošanu kā aromatizētājs pārstrādātos pārtikas produktos, tas ir, vielās, kas imitē dabiskajam ēdienam raksturīgo garšu un aromātu, piemēram, augļiem. Turklāt esterus joprojām izmanto zāļu, kosmētikas, smaržu un vasku ražošanā.
Autors: Diogo Lopes Dias
Avots: Brazīlijas skola - https://brasilescola.uol.com.br/o-que-e/quimica/o-que-e-ester.htm
