Iedomājieties, ka pievienojat 10 g galda sāls (nātrija hlorīds - NaCl) glāzē ar 100 g ūdens 20 ° C temperatūrā. Pēc sajaukšanas jūs redzat, ka sāls ir pilnībā izšķīdis, tāpēc jūs nolemjat pievienot vēl vairāk sāls. Kādā brīdī jūs vairs nevarēsit izšķīdināt sāli šajā ūdens daudzumā, un pievienotā sāls nogrims glāzes apakšā, lai arī kā jūs mēģinātu to sajaukt.
Kad tas notiek, mēs sakām, ka risinājums ir piesātināts un ka šķīdības koeficients. Tāpēc mēs varam noteikt šķīdības koeficientu šādi:
“Šķīdības koeficients ir maksimālais izšķīdušās vielas daudzums, kas tiek izšķīdināts noteiktā šķīdinātāja daudzumā noteiktā temperatūrā. ”
Piemēram, sāls šķīdības koeficients ūdenī ir vienāds ar 36 g NaCl / 100 g ūdens 20 ° C temperatūrā. Šajā ūdens daudzumā un šajā temperatūrā nav iespējams izšķīdināt papildu gramu sāls, kā šķīdības koeficients katrai vielai ir specifisks. Ja mēs mainām izšķīdušo vielu, piemēram, aizstājot galda sāli ar NH4Cl, tā šķīdības koeficients ir vienāds ar 37,2 g 100 g ūdens 20 ° C temperatūrā.
Turklāt tai pašai vielai ir dažādas šķīdības dažādos šķīdinātājos. Kamēr sāls šķīst ūdenī, tas praktiski nešķīst acetonā vai etilacetātā (šķīdinātājs, ko izmanto glazūru noņemšanai).
Vēl viens punkts ir tāds, ka vienmēr, kad tiek pieminēts izšķīdušās vielas šķīdības koeficients noteiktā šķīdinātāja daudzumā, ir arī jānorāda temperatūra, jo tas ir traucējošs faktors. Piemēram, ja ņemam 100 g ūdens 20 ° C temperatūrā un pievienojam 40 g sāls, 36 g izšķīdīs un 4 g veidosies nogulsnes. Bet, ja mēs izmantosim šo risinājumu apkurei, mēs redzēsim, ka 4 g izšķīdīs, paaugstinoties temperatūrai.
Tas mums parāda, ka tai pašai šķīdinātai vielai, kas izšķīdināta tajā pašā šķīdinātāja daudzumā, temperatūras paaugstināšanās laikā ir atšķirīgi šķīdības koeficienti.
Skatiet piemēru zemāk:
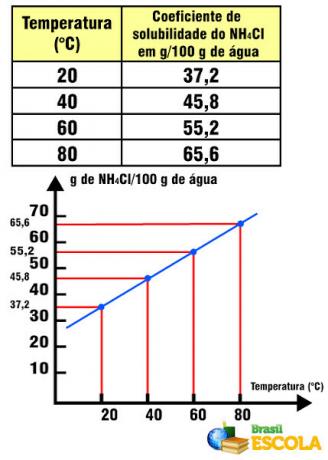
NH šķīdības koeficients4Cl attiecībā pret temperatūru
Jāņem vērā, ka šajā gadījumā NH šķīdības koeficients4Cl palielinās, palielinoties temperatūrai. Tas notiek ar lielāko daļu sāļu ūdenī. Tomēr ir situācijas, kurās šķīdības koeficients samazinās, palielinoties temperatūrai, tāpat kā Ce gadījumā2(TIKAI4)3. Ir arī gadījumi, kad šķīdības koeficientā nav tik izteiktas mainības, kā tas notiek ar galda sāli. Skatiet to tekstā Šķīdības līkņu grafiki.
Var gadīties, ka zināmās specifiskās situācijās mēs varam šķīdinātājā izšķīdināt arī izšķīdušās vielas daudzumu, kas lielāks par tā šķīdības koeficientu, tādējādi iegūstot t.s. pārsātināts šķīdums. Piemēram, iedomājieties, ka šķīdums, kas izveidots ar 100 g ūdens 20 ° C temperatūrā un 40 g galda sāls (ar 36 g izšķīdis un 4 g nogulsnēts), karsē, līdz tas sasniedz visu izšķīdušās vielas temperatūru izšķīdināt sevi. Tad šo šķīdumu atstāj atpūsties, lai tas atdziest, līdz tas sasniedz istabas temperatūru, kas ir tuvu 20 ° C.
Ja šķīdumā nav traucējumu, papildu izšķīdušā viela paliks izšķīdināta, tādējādi veidojot pārsātinātu šķīdumu. Tomēr šāda veida šķīdums ir ļoti nestabils, un jebkura pēkšņa kustība var izraisīt kristalizāciju daudzumā, kas pārsniedz šķīdības koeficientu. Tādējādi risinājums, kas bija pārsātināts kļūs piesātināts ar fona ķermeni.
Pēdējais gadījums ir nepiesātināts šķīdums, kas ir tad, kad izšķīdušās izšķīdušās vielas daudzums ir mazāks par šķīdības koeficienta vērtību. Piemērs ir 10 g NaCl izšķīdināšana 100 g ūdens 20 ° C temperatūrā.
Autore Jennifer Fogaça
Beidzis ķīmiju
Avots: Brazīlijas skola - https://brasilescola.uol.com.br/quimica/coeficiente-solubilidade.htm
