O Etiķskābe ir bezkrāsains šķidrums ar kairinošu un iekļūstošu smaržu un skābu garšu, ko ķīmiski sauc etānskābe un tā strukturālā formula ir parādīta zemāk:
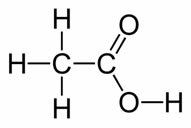
Skatiet, ka tas ir savienojums, kas pieder organiskajai grupai karbonskābes.
Viņš ir galvenais etiķis, kas ir ūdens šķīdums no 4 līdz 10 masas% etiķskābes. To pirmo reizi ieguva, izmantojot vīna etanolu, kas oksidējas ar gaisā esošo skābekli. No tā izriet arī tā nosaukums, jo skābais vīns nāk no latīņu valodas acetum kas nozīmē “etiķis”.
Šī savienojuma izmantošana ir ļoti sena, ieskaitot romiešu leģionus, kas iekaroja lielu daļu pasaules, kas bija pazīstami 3. gadsimtā pirms mūsu ēras. C., devās garos attālumos un nesa sev līdzi kolbu ar atšķaidītu skābu vīnu. Šis etiķskābes maisījums stimulēja karavīru siekalošanos un mazināja slāpju sajūtu.

Mūsdienās šīs skābes ražošanai nozare parasti izmanto to pašu principu, tas ir, etanola (etilspirta) oksidēšanu:
H3C CH2 ─ OH + O2 (gaiss) → H3C COOH + H2O
Etanola skābeklis etiķskābe vai etānskābe Ūdens
Etiķa gadījumā šī oksidēšanās, kas parādīta iepriekšminētajā ķīmiskajā reakcijā, tiek iegūta fermentējot, izmantojot sēnīti Mycoderma aceti (sauca etiķa māte) un spirta oksidāzes enzīms. Varat arī izmantot ģints baktērijas Acetobaktērija un Clostridium acetobtylicum. Tomēr vēl viens līdzeklis ir tāda katalizatora kā divanādija pentoksīda (V2O5).
Etiķskābi var ražot arī oksidējot metanolu, destilējot koksni un izmantojot naftas atvasinājumus.
Etiķskābi papildus izmantošanai kā garšvielu pārtikā izmanto arī vinilacetāta (PVA polimēra ražošanai), etiķskābes anhidrīda un acetilhlorīds (izmantots organiskās sintēzēs), esteru (šķīdinātāji, smaržas, esences, cita starpā), celulozes acetāta (tekstilšķiedras), acetātu neorganiskās vielas utt.
Kad tas ir tīrā formā, to sauc ledus etiķskābe, jo tas sacietē 16,7 ° C temperatūrā, piešķirot tam ledus izskatu.

Autore Jennifer Fogaça
Beidzis ķīmiju

