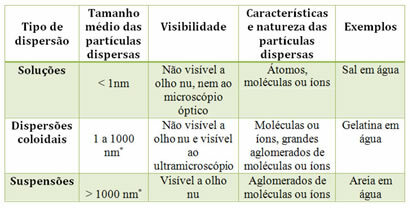
Sagatavojot šķīdumu, tas ir, izšķīdinot izšķīdušo vielu noteiktā šķīdinātājā, izšķīdušās vielas molekulas vai joni atdalās, paliekot izkliedēti šķīdinātājā.
Mēs varam noteikt attiecības starp dažādām izšķīdušajām vielām un to ūdens šķīdumu īpašībām, izmantojot ļoti vienkāršus eksperimentus, ko veic tajā pašā temperatūrā. Ņemiet vērā šādas situācijas:
THE)
B)
Kamēr mēs skatāmies uz risinājumiem THE un B, mēs pamanījām, ka sāls ir mazāk šķīstošs nekā cukurs, un, pamatojoties uz šo faktu, mēs varam vispārināt:
Piesātināts šķīdums: ir tas, kas satur maksimālo izšķīdušās vielas daudzumu noteiktā šķīdinātāja daudzumā noteiktā temperatūrā; sakarību starp maksimālo izšķīdušās vielas daudzumu un šķīdinātāja daudzumu sauc par šķīdības koeficientu. Piemērs: maksimālais sāls (NaCl) daudzums, kas izšķīst 100 g H220°C temperatūrā tas ir 36 g; šķīdumu sauc par piesātinātu.
Šķīdumu, kurā izšķīdušās vielas daudzums ir mazāks par šķīdības koeficientu, sauc par šķīdumu. nepiesātināts vai nepiesātināts.
Nepārtrauciet tagad... Pēc reklāmas ir vēl kas ;)
Risinājumi - Fizikāli ķīmiskais
Ķīmija - Brazīlijas skola
Vai vēlaties atsaukties uz šo tekstu kādā skolā vai akadēmiskajā darbā? Skaties:
SKOLA, Brazīlijas komanda. "Šķīdība un šķīdības līknes"; Brazīlijas skola. Pieejams: https://brasilescola.uol.com.br/quimica/solubilidade-curvas-solubilidade.htm. Skatīts 2021. gada 27. jūlijā.