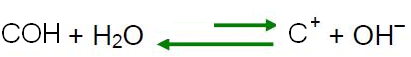
Vide tiek uzskatīta par neitrālu, ja tajā ir tāda pati hidronija jonu koncentrācija mol/l (H3O+) un hidroksīds (OH-).
Neitrālas vides piemērs, kas pat kalpo kā standarts citiem šķīdumiem, ir tīrs, destilēts ūdens 25ºC temperatūrā. Šajā temperatūrā tai ir tieši 1. 10-7 mol/L abu jonu. Tādējādi jūsu jonu produkts (Kw) ir vienāds ar 10-14 (mol/l)2:
Kw = [H3O+]. [ak-]
Kw = (1. 10-7 mol/l). (1. 10-7 mol/l) = 10-14 (mol/l)2
PH un pOH ir norādīti zemāk:
pH= - log [H3O+] pOH= -log[OH-]
pH= - log 1. 10-7 pOH= - log 1. 10-7
pH = 7pOH = 7
Tas parāda, ka neitrālā risinājumā pH ir vienāds ar pOH.
- Skāba vide:
Skābā vidē H jonu koncentrācija3O+ ir lielāks nekā OH joniem-.
Šādu risinājumu var panākt, pievienojot nelielu daļu H jonu3O+piemēram, ar skābes palīdzību.
Saskaņā ar Le Šateljē principu, kad līdzsvara sistēmā tiek radīts traucējums, tai ir tendence pārregulēties, lai samazinātu šī spēka ietekmi. Tas nozīmē, ka, ja ūdenim pievieno skābi, H joni3O+ tie būs pāri un līdzsvars nobīdīsies apgrieztās reakcijas virzienā, pa kreisi. Tātad šie liekie joni reaģēs ar OH joniem
-. Tādējādi OH jonu koncentrācija- samazināsies un šķīdums kļūs skābs.
Jonu reizinājums (Kw) vienmēr ir vienāds ar 10-14, bet H jonu koncentrācija3O+ ir lielāka par OH jonu koncentrāciju-1. Tāpēc pH ir lielāks par pOH skābā vidē, bet tā summa vienmēr ir vienāda ar 14.
Turklāt, jo lielāka ir H jonu koncentrācija3O+, jo lielāka ir pH vērtība. Istabas temperatūrā (25°C), pH < 7 un pOH > 7.

- Pamatlīdzekļi:
Pamatvidē OH jonu koncentrācija- ir lielāks nekā H jonu3O+.
Ja mēs pievienojam ūdenim bāzi, tas nozīmē, ka mēs pievienojam OH jonus.- un, kā paskaidrots iepriekšējā punktā, pēc Le Šateljē principa, reakcijas līdzsvars ūdens pašjonizācija virzīsies pretējā virzienā, jonu pārpalikumam reaģējot ar H joni3O+, samazinot koncentrāciju un padarot šķīdumu bāzisku.
Tādā gadījumā pOH būs lielāks par pH. Istabas temperatūrā (25°C), pH > 7 un pOH < 7.

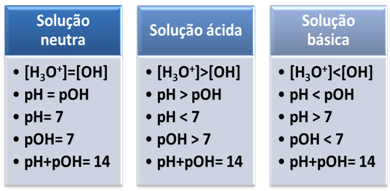
Īsumā:
Autore: Dženifera Fogača
Beidzis ķīmiju


