O vienādojuma līdzsvarošana ļauj mums saskaņot ķīmisko vienādojumu klātesošo atomu skaitu tā, lai tas kļūtu patiess un atspoguļotu ķīmisko reakciju.
Izmantojiet zemāk minētos jautājumus, lai pārbaudītu savas zināšanas un pārbaudītu atbildes, kas komentētas pēc atsauksmēm, lai atbildētu uz jūsu jautājumiem.
jautājums 1
(Makenzija-SP)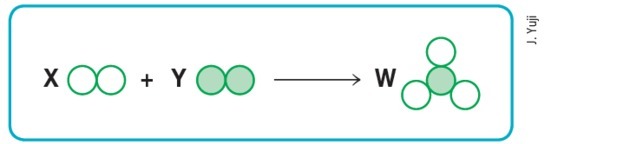
Pieņemot, ka tukšie un aizpildītie apļi attiecīgi nozīmē dažādus atomus, tad shēma augstāk parādīs līdzsvarotu ķīmisko reakciju, ja burtus X, Y un W aizstāsim attiecīgi ar vērtības:
a) 1, 2 un 3.
b) 1, 2 un 2.
c) 2, 1 un 3.
d) 3, 1 un 2.
e) 3, 2 un 2.
D) alternatīva 3, 1 un 2.
1. solis: Mēs piešķiram burtus, lai vienādojumu būtu vieglāk saprast.
2. solis: mēs saskaitām indeksus, lai uzzinātu, kuram vienādojumā ir visvairāk atomu.
| B |
Katrā vienādojuma loceklī A un B parādās tikai vienu reizi. Tomēr, ja saskaita indeksus, redzam, ka A ir visaugstākā vērtība. Tāpēc mēs sākām viņam līdzsvarošanu.
3. solis: Mēs līdzsvarojam elementu A, transponējot indeksus un pārvēršot tos koeficientos.
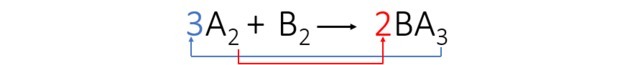
Mēs novērojām, ka elements B tika automātiski līdzsvarots un vienādojuma koeficienti ir: 3, 1 un 2.
2. jautājums
(Unicamp-SP) Izlasiet nākamo teikumu un pārveidojiet to (līdzsvarotā) ķīmiskajā vienādojumā, izmantojot simbolus un formulas: “gāzveida slāpekļa molekula, kas satur divus slāpeklis uz vienu molekulu, reaģē ar trim gāzveida diatomiskā ūdeņraža molekulām, iegūstot divas gāzveida amonjaka molekulas, kas sastāv no trim ūdeņraža atomiem un viena no slāpeklis ".
Atbildēt:
Pārstāvot jautājumā aprakstītos atomus, mēs varam saprast, ka reakcija notiek šādi:
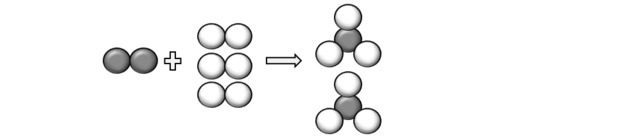
Tātad mēs nonākam pie vienādojuma:
3. jautājums
Ūdeņraža peroksīds ir ķīmisks savienojums, kas var sadalīties, veidojot ūdeni un skābekli, saskaņā ar zemāk esošo ķīmisko vienādojumu.
Attiecībā uz šo reakciju pareizi līdzsvarotais vienādojums ir:
a) H2O2 →2 + H2O
b) 2 stundas2O2 →2 + 2H2O
c) H2O2 → 2O2 + H2O
d) 2H2O2 → 2O2 + 2H2O
Pareiza alternatīva: b) 2H2O2 →2 + 2H2O
Ņemiet vērā, ka ūdeņraža peroksīds ir ķīmiska viela, kas sastāv no divu ķīmisko elementu atomiem: ūdeņraža un skābekļa.
Pēc sadalīšanās reakcijas jums ir jābūt vienādam abu elementu atomu skaitam gan reaģentos, gan produktos. Lai to izdarītu, mums ir jālīdzsvaro vienādojums.
Ņemiet vērā, ka mums reaģentā ir 2 ūdeņraža atomi (H2O2) un produktā divi atomi (H2O). Tomēr skābeklim reaģentā ir divi atomi (H2O2) un trīs atomi produktos (H2O un O2).
Ja koeficientu 2 ieliekam pirms ūdeņraža peroksīda, mēs dubultojam atomu skaitu elementos.
Ņemiet vērā, ka, ja mēs ievietojam to pašu koeficientu kopā ar ūdens formulu, mums abās pusēs ir vienāds atomu daudzums.
Tāpēc pareizi līdzsvarots ķīmiskais vienādojums ir 2H2O2 →2 + 2H2O.
4. jautājums
(UFPE) Apsveriet tālāk norādītās ķīmiskās reakcijas.
Mēs varam teikt, ka:
a) visi ir līdzsvaroti.
b) 2, 3 un 4 ir līdzsvaroti.
c) tikai 2 un 4 ir līdzsvaroti.
d) tikai 1 nav līdzsvarots.
e) neviens nav pareizi sabalansēts, jo reaģentu un produktu fizikālais stāvoklis ir atšķirīgs.
B) alternatīva 2, 3 un 4 ir līdzsvarota.
1. un 5. alternatīva ir nepareiza, jo:
- 1. vienādojums nav līdzsvarots, pareizais līdzsvars būtu:
- 5. vienādojums nav pareizs, jo reakcijā izveidojies savienojums būtu H2TIKAI3.
Lai izveidotu H2TIKAI4 jāiekļauj SO oksidēšanas vienādojumā2.
5. jautājums
(Mackenzie-SP) Uzkarsēts līdz 800 ° C, kalcija karbonāts sadalās kalcija oksīdā (neapstrādātā kaļķā) un oglekļa dioksīdā. Pareizi līdzsvarotais vienādojums, kas atbilst aprakstītajai parādībai, ir:
(Dots: Ca - sārma zemes metāls.)
C) alternatīva
Kalcijs ir sārmzemju metāls, un kalcija stabilitātei ir vajadzīgi 2 elektroni (Ca2+), kas ir skābekļa lādiņš (O2-).
Tādējādi kalcija atoms saistās ar skābekļa atomu, un izveidotais savienojums ir CaO, kas ir nedzīvs kaļķis.
Otrs produkts ir oglekļa dioksīds (CO2). Abus veido kalcija karbonāts (CaCO3).
Ievietojot to vienādojumā:
Mēs atzīmējam, ka atomu daudzums jau ir pareizs un nav nepieciešams līdzsvarot.
6. jautājums
(UFMG) Vienādojums nav līdzsvarots. Balansējot to ar pēc iespējas mazākiem skaitļiem, stehiometrisko koeficientu summa būs:
a) 4
b) 7
c) 10
d) 11
e) 12
E) alternatīva 12
Izmantojot izmēģinājuma metodi, līdzsvarošanas secība būs:
1. solis: Tā kā elements, kas katrā dalībniekā parādās tikai vienu reizi un kuram ir visaugstākais indekss, ir kalcijs, mēs sākām tam līdzsvarot.
2. solis: Mēs sekojam radikālās PO līdzsvarošanai43-, kas arī parādās tikai vienu reizi.
3. solis: mēs līdzsvarojam ūdeņradi.
Ar to mēs novērojam, ka automātiski tika pielāgots skābekļa daudzums un vienādojuma bilance ir:
Atceroties, ka tad, kad koeficients ir 1, tas nav jāraksta vienādojumā.
Pievienojot koeficientus, kas mums ir:
7. jautājums
Sadegšana ir ķīmiskās reakcijas veids, kurā enerģija tiek izdalīta siltuma formā.
Pilnībā sadedzinot vielu, ko veido ogleklis un ūdeņradis, veidojas oglekļa dioksīds un ūdens.
Novērojiet ogļūdeņraža sadegšanas reakcijas un atbildiet, kurš no zemāk redzamajiem vienādojumiem ir nepareizi līdzsvarots:
a) CH4 + 2O2 → CO2 + 2H2O
b) C3H8 +502 → 3CO2 + 4H2O
c) C4H10 + 13 / 3O2 → 4CO2 + 5h2O
d) C2H6 + 7 / 2O2 → 2CO2 + 3H2O
Nepareiza atbilde: c) C4H10 + 13 / 3O2 → 4CO2 + 5h2O
Lai līdzsvarotu ķīmiskos vienādojumus, vispirms apskatīsim, kurš elements katrā vienādojuma loceklī parādās tikai vienu reizi.
Ņemiet vērā, ka ogleklis un ūdeņradis katrā sniegtajā vienādojumā veido tikai vienu reaģentu un vienu produktu.
Tātad sāksim līdzsvarot ar ūdeņradi, jo tajā ir lielāks atomu skaits.
Tāpēc balansēšanas secība būs:
- Ūdeņradis
- Ogleklis
- Skābeklis
Ūdeņradis
Tā kā produktā ir 2 ūdeņraža atomi, mēs ievietojam skaitli kā koeficientu, kas reizināts ar 2, iegūst reaģenta ūdeņraža atomu skaitu.
a) CH4 + O2 → CO2 + 2H2O
b) C3H8 + O2 → CO2 + 4H2O
c) C4H10 + O2 → CO2 + 5H2O
d) C2H6 + O2 → CO2 + 3H2O
Ogleklis
Balansēšanu veic, transponējot oglekļa indeksu reaģentā un izmantojot to kā koeficientu produktam, kurā ir šī elementa atomi.
a) CH4 + O2 → 1CO2 + 2H2O
b) C3H8 + O2 → 3CO2 + 4H2O
c) C4H10 + O2 → 4CO2 + 5h2O
d) C2H6 + O2 → 2CO2 + 3H2O
Skābeklis
Pievienojot skābekļa atomu skaitu izveidotajos produktos, mēs atrodam elementa atomu skaitu, kam jāreaģē.
Lai to izdarītu, mums kā koeficientu jāievieto skaitlis, kas reizināts ar 2 rada skābekļa atomu skaitu produktos.
a) CH4 + O2 → 1CO2 + 2H2O
2x = 2 + 2
2x = 4
x = 2
Tātad pareizais vienādojums ir: CH4 + 2O2 → 1CO2 + 2H2O.
b) C3H8 + O2 → 3CO2 + 4H2O
2x = 6 + 4
2x = 10
x = 5
Tātad pareizais vienādojums ir: C3H8 + 5O2 → 3CO2 + 4H2O
c) C4H10 + O2 → 4CO2 + 5h2O
2x = 8 + 5
2x = 13
x = 13/2
Tātad pareizais vienādojums ir: C4H10 + 13/2O2 → 4CO2+ 5h2O
d) C2H6 + O2 → 2CO2 + 3H2O
2x = 4 + 3
2x = 7
x = 7/2
Tātad pareizais vienādojums ir: C2H6 + 7/2O2 → 2CO2 + 3H2O
Pareizi līdzsvaroti vienādojumi ir:
a) CH4 + 2O2 → CO2 + 2H2O
b) C3H8 +502 → 3CO2 + 4H2O
c) C4H10 + 13 / 2O2 → 4CO2 + 5h2O
d) C2H6 + 7 / 2O2 → 2CO2 + 3H2O
Tādējādi alternatīva c) C4H10 + 13 / 3O2 → 4CO2 + 5h2Lieta ir tāda, ka tai nav pareizā līdzsvara.
8. jautājums
(Enem 2015) Kaļķakmeņi ir materiāli, kas sastāv no kalcija karbonāta, kas var darboties kā sēra dioksīda (SO2), kas ir svarīgs gaisa piesārņotājs. Procesā iesaistītās reakcijas ir kaļķakmens aktivācija kalcinēšanas ceļā un SO fiksācija2 ar kalcija sāls veidošanos, kā to ilustrē vienkāršotie ķīmiskie vienādojumi.
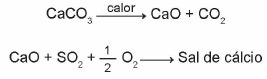
Ņemot vērā reakcijas, kas saistītas ar šo desulfurizācijas procesu, kalcija sāls ķīmiskā formula atbilst:
B) alternatīva
Tā kā reakcija ir līdzsvarota, reaģentos esošajiem atomiem produktos jābūt tādā pašā daudzumā. Tādējādi
Izveidoto sāli veido:
1 kalcija atoms = Ca
1 sēra atoms = S
4 skābekļa atomi = O4
Tāpēc kalcija sāls ķīmiskā formula atbilst CaSO4.
9. jautājums
(UFPI) X reakcija ar Y ir parādīta zemāk. Nosakiet, kurš vienādojums vislabāk atspoguļo līdzsvaroto ķīmisko vienādojumu.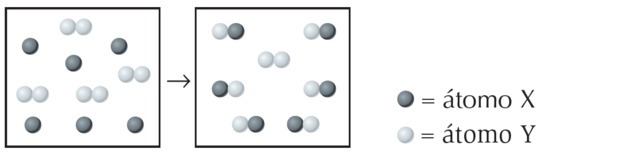
A) alternatīva
Attēlā mēs novērojam, ka suga X ir viens atoms, savukārt Y ir diatomisks, tas ir, tas veidojas, savienojot 2 atomus. Tātad X reaģē ar Y2.
Izveidoto produktu attēlo XY, vienādojums nav līdzsvarots:
Mēs līdzsvarojam vienādojumu šādi:
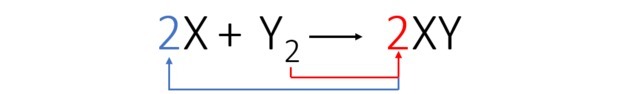
Saskaņā ar līdzsvaroto vienādojumu zemāk redzamais skaitlis parāda, kā notiek reakcija un tās proporcija.
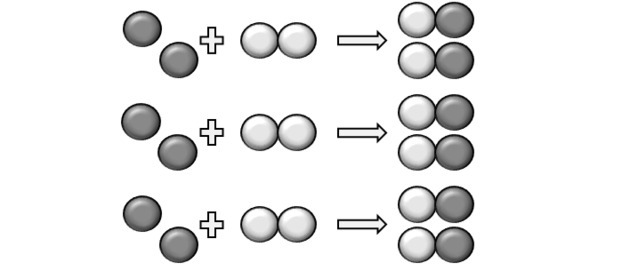
Lai notiktu reakcija, jābūt fiksētai attiecībai, un tāpēc daži savienojumi var nereaģēt. Tas ir tas, ko parāda attēls, jo produktā mēs redzam, ka Y2 nereaģēja.
10. jautājums
(Enem 2010) Aizvien biežāk notiek mobilizācija, lai veicinātu labāku planētu nākamajām paaudzēm. Lielākā daļa masu transporta līdzekļu šobrīd tiek darbināti ar fosilā kurināmā sadedzināšanu. Kā piemēru šīs prakses radītajam slogam ir pietiekami zināt, ka automašīna vidēji saražo aptuveni 200 g oglekļa dioksīda uz nobraukto km.
Globālās sasilšanas žurnāls. 2., 8. gads. Instituto Brasileiro de Cultura Ltda publikācija.
Viena no galvenajām benzīna sastāvdaļām ir oktāns (C8H18). Degot oktānskaitļa enerģijai, ir iespējama automašīnas kustība. Vienādojums, kas attēlo šī procesa ķīmisko reakciju, parāda, ka:
a) procesā izdalās skābeklis O formā2.
b) stehiometriskais koeficients ūdenim ir 8 līdz 1 oktānskaitlis.
c) procesā notiek ūdens patēriņš, tāpēc tiek atbrīvota enerģija.
d) skābekļa stehiometriskais koeficients ir 12,5 līdz 1 oktāns.
e) oglekļa dioksīda stehiometriskais koeficients ir 9 līdz 1 oktāns
D) alternatīva) skābekļa stehiometriskais koeficients ir 12,5 līdz 1 oktāns.
Līdzsvarojot vienādojumu, mēs atrodam šādus koeficientus:
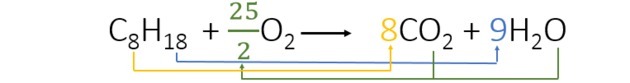
- Mēs sākām balansēšanu ar ūdeņradi, kas katrā loceklī parādās tikai vienu reizi un kuram ir lielāks indekss. Tā kā ir 18 reaģējoši ūdeņraža atomi, produktā ir 2, tāpēc mums jāpievieno skaitlis, kas reizināts ar 2, dod 18. Tātad koeficients ir 9.
- Tad mēs pievienojam koeficientu 8 CO priekšā2 lai katrā vienādojuma loceklī būtu 8 ogles.
- Visbeidzot, vienkārši pievienojiet skābekļa daudzumu produktā un atrodiet vērtību, kas reizināta ar 2, dod mums 25 skābekļa atomus. Tātad mēs izvēlējāmies 25/2 vai 12.5.
Tādējādi 1 oktāna sadedzināšanai tiek patērēts 12,5 skābeklis.
11. jautājums
(Fatec-SP) Būtiska mēslošanas līdzekļu īpašība ir to šķīdība ūdenī. Tāpēc mēslojuma rūpniecība pārveido kalcija fosfātu, kura šķīdība ūdenī ir ļoti zema, par daudz labāk šķīstošu savienojumu, kas ir kalcija superfosfāts. Šo procesu attēlo vienādojums:
kur x, y un z vērtības ir attiecīgi:
a) 4, 2 un 2.
b) 3, 6 un 3.
c) 2, 2 un 2.
d) 5, 2 un 3.
e) 3, 2 un 2.
E) alternatīva 3, 2 un 2.
Izmantojot algebrisko metodi, mēs veidojam vienādojumus katram elementam un vienādojam reaktorā esošo atomu skaitu ar produkta atomu skaitu. Tādēļ:
Līdzsvarots vienādojums:
12. jautājums
Līdzsvarojiet zemāk esošos vienādojumus, izmantojot izmēģinājuma metodi.
Atbildēt:
Vienādojumu veido ūdeņraža un hlora elementi. Mēs līdzsvarojam elementus, tikai pievienojot koeficientu 2 produkta priekšā.
Vienādojums nebija jāsabalansē, jo atomu daudzums jau ir koriģēts.
Fosforam reaģentos ir divi atomi, tāpēc, lai līdzsvarotu šo elementu, fosforskābes daudzumu produktā noregulējam uz 2H3Putekļi4.
Pēc tam mēs novērojām, ka ūdeņradim produktā ir 6 atomi, mēs līdzsvarojām šī elementa daudzumu, pievienojot koeficientu 3 reaktantam, kas to satur.
Veicot iepriekšējās darbības, skābekļa daudzums tika koriģēts.
Aplūkojot vienādojumu, mēs redzam, ka ūdeņraža un broma daudzums produktos ir divreiz lielāks nekā ja reaģentos ir, HBr pievienojam koeficientu 2, lai līdzsvarotu šos divus elementi.
Hlora produktos ir 3 atomi un reaģentos ir tikai 1, tāpēc mēs līdzsvarojam koeficienta 3 noteikšanu pirms HCl.
Ūdeņraža reaģentos bija 3 un produktos - 2 atomi. Lai pielāgotu lielumus, mēs pārveidojam H indeksu2 koeficientā mēs reizinām ar 3, kas jau bija HCl, un iegūstam rezultātu 6HCl.
Pielāgojam hlora daudzumu produktos, lai tajā būtu arī 6 atomi un iegūtu 2AlCl3.
Alumīnija izstrādājumos bija 2 atomi, mēs reaģentos pielāgojām daudzumu 2Al.
Mēs līdzsvarojam ūdeņraža daudzumu produktā līdz 3H2 un mēs pielīdzinām šī elementa 6 atomu daudzumu katrā vienādojuma izteiksmē.
Vienādojumā nitrāta radikāls (NO3-) produktā ir indekss 2, mēs pārveidojam indeksu koeficientā 2AgNO reaģentā3.
Sudraba daudzums bija jāpielāgo, jo tā reaģentos tagad ir 2 atomi, tāpēc mums produktā ir 2Ag.
Reaģentos mums ir 4 ūdeņraža atomi, un, lai līdzsvarotu šo elementu, HCl produktam pievienojam koeficientu 2.
Hlora produktos tagad ir 4 atomi, tāpēc mēs reaģenta daudzumu noregulējam uz 2Cl2.
Reaģentos ir 6 ūdeņraža atomi, un, lai līdzsvarotu šo elementu, ūdens daudzumu noregulējam uz 3H2O.
Reaģentos mums ir 2 oglekļa atomi, un, lai līdzsvarotu šo elementu, mēs noregulējam oglekļa dioksīda daudzumu līdz 2CO2.
Skābekļa reaģentos jābūt 7 atomiem, un, lai līdzsvarotu šo elementu, molekulārā skābekļa daudzumu noregulējam uz 3O2.
Aplūkojot vienādojumu, nitrāta radikāls (NO3-) produktā ir indekss 2. AgNO reaģentā indeksu pārveidojam par koeficientu 23.
Reaģentos mums ir 2 sudraba atomi, un, lai līdzsvarotu šo elementu, mēs pielāgojam sudraba hlorīda daudzumu produktā līdz 2AgCl.
Produktā ir 3 kalcija atomi, un, lai līdzsvarotu šo elementu, kalcija nitrāta daudzumu reaģentā noregulējam uz 3Ca (NO3)2.
Pēc tam mums paliek 6 NO radikāļi3- reaģentos un lai līdzsvarotu šo radikāļu, mēs noregulējam slāpekļskābes daudzumu produktos līdz 6HNO3.
Tagad produktos ir 6 ūdeņraža atomi, un, lai līdzsvarotu šo elementu, fosforskābes daudzumu reaģentā noregulējam uz 2H3Putekļi4.
Uzziniet vairāk par aprēķiniem ar ķīmiskiem vienādojumiem:
- Ķīmisko vienādojumu līdzsvarošana
- Stehiometrija
- Stehiometriskie aprēķini
- Stehiometrijas vingrinājumi
- Periodiskās tabulas vingrinājumi
