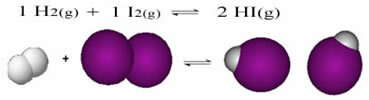
Strukturālā formula ir shēma, kas norāda struktūru, tas ir, atomu izvietojumu, kas veido ķīmiskos elementus, kā arī savienojumu starp tiem. To var attēlot dažādos veidos: plakans, kondensēts vai elektronisks.
Starp faktoriem, kas nosaka izmantotās struktūras, elektronu skaits valences apvalkā ir viens no tiem.
Plakana formula
Plakanā formula izmanto domuzīmes, lai attēlotu kovalentās saites, kas var būt vienas, dubultas vai trīskāršas un attēlotas šādos veidos:
- vienkāršs savienojums (kad dalās 2 elektroni)
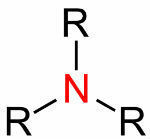
= dubultā saite (kad tiek dalīti 4 elektroni)
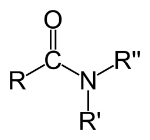
≡ trīskāršā saite (kad dalās 6 elektroni)
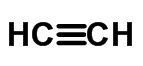
Saīsināta vai vienkāršota formula
Kondensētajā strukturālajā formulā saites nav parādītas.
Attēlā katra elementa atomu skaits ir norādīts saīsināti, tas ir, vienkāršoti:
H3C CH2 CH2 CH3
Lineārā kondensētā formula
Lineārajā kondensētajā formulā tiek izmantotas zigzaga līnijas, kuru virsotnēs ir attēloti ogļi:
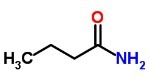
Elektroniskā vai Lūisa formula
Elektronisko formulu, sauktu arī par Lūisa formulu, attēlo punkti.
Caur šiem punktiem tiek parādīti elektronu daudzumi, kas atrodas valences slāņos:
H: H
Un molekulārā formula?
molekulārā formula, neatsaucoties uz tā struktūru, norāda elementu skaitu, kas veido a molekula. Papildus tam, lai norādītu katrā elementā esošo atomu skaitu un to proporcijas.
To var iegūt, izmantojot minimālo vai empīrisko formulu un procentuālo vai centesimālo formulu.
Lasīt arī Izomērija un Valensijas slānis.
Atrisināti vingrinājumi
1. (Vunesp-2000) Uzrakstiet strukturālo formulu un norādiet oficiālo nosaukumu:
a) piesātināts sazarots oglekļa ķēdes ketons ar 7 oglekļa atomiem.
b) aminoskābe ar 4 oglekļa atomiem.
)

B)
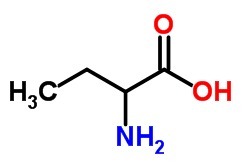
2. (FGV-2005) Aspartāms ir mākslīgs saldinātājs, kuru nejauši 1965. gadā atklāja neuzmanīgs ķīmiķis, kurš laizīja savus netīros pirkstus un jutās, ka tie ir saldi.
Šie nehigiēniskie ieradumi nav ieteicami, jo daudzas vielas minūtēs ir ļoti toksiskas.
Aspartāma strukturālā formula ir parādīta zemāk:

No aspartāma strukturālās formulas šķiet, ka ir
a) 13 oglekļa atomi uz molekulu.
b) 1 ētera funkcionālā grupa.
c) 1 dipeptīds
d) 2 terciārie oglekļa atomi
e) tikai 1 asimetrisks oglekļa atoms.
C) alternatīva: 1 dipeptīds
Lai turpinātu pārbaudīt savas zināšanas, skatiet arī šos vingrinājumu sarakstus:
- Vingrinājumi ogļūdeņražiem
- Organiskās ķīmijas vingrinājumi
- Vingrinājumi par plakanu izomēriju