Plkst hidratācijas reakcijas alkadiēni viņi ir pievienošanas reakcijas, tas ir, ūdens molekulas sastāvdaļas (hidronijs un hidroksīds) pievieno alkadiēnam.
Jūs alkadiēni ir ogļūdeņraži, kuriem ir atvērta ķēde un divas oglekļa savienojumi (ko veido sigma un pi), kā redzams šādā struktūrā:

Alkadiēna strukturālā formula
priekš hidratācijas reakcija alkadienos tiek veikts, ir svarīgi, lai pi saite, kas atrodas divkāršā saitē, siltuma un sērskābes (H2TIKAI4). Pārtraucot pi saiti, parādās divas saites vietas, katra no tām uz vienu no oglekļiem, kas saistīti ar dubulto saiti.

Saistīšanās vietu parādīšanās ar pi saistīšanas traucējumiem
Saistīšanās vietu parādīšanās uz alkadiēna molekulas ir nepieciešama joniem (H+ un ak-) no ūdens pievieno alkadiēnam, veidojot, piemēram, dialkolu (alkohols ar diviem hidroksiliem).
H pievienošana+ un ak- alkadiēna struktūrā
PIEZĪME: H pievienošana+ un ak- alkadiēna struktūrā seko Markovņikova valdīšana, ti, H+ saistās ar visvairāk hidrogenēto oglekli un OH- saistās ar mazāk hidrogenētu oglekli.

Piemērs Markovņikova noteikuma piemērošanai alkadiēnu hidratācijā
Tā kā attiecībā uz dubulto saišu stāvokli ir dažādi alkadiēnu veidi, var būt, ka alkadiēna hidratācija veido dažādus savienojumus. Skatiet šādus gadījumus:
→ Uzkrātais vai kondensētais alkadiēns
Tas ir alkadiēns, kuram ir divas dubultās saites, vienlaikus iesaistot trīs atomus ogleklis, tas ir, nav vienas saites, kas atdala saitēs iesaistītos oglekļus dubultspēles.

Uzkrāta alkadiēna strukturālā formula
Mainīga alkadiēna hidratācijas reakcijas laikā pi saites tiek sadalītas, kas ir H+ pievieno vairāk hidrogenētiem oglekļiem un OH- pievieno mazāk hidrogenētiem oglekļiem:
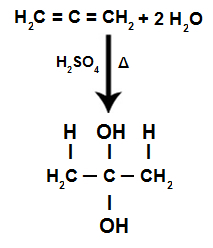
Uzkrātais alkadiēna hidratācijas reakcijas vienādojums
Mums ir tāds, ka uzkrāta alkadiēna hidratācijā viens un tas pats oglekļa atoms saņem abus hidroksilus, veidojot dvīņu spirtu, kas ir nestabila struktūra.

Dvīņu veidotā spirta struktūra
Tā kā dvīņu spirts ir nestabils, mums ir izveidojusies ūdens molekula ar abu hidroksilu komponentiem un izveidota pi saite starp oglekli un skābekli.

Ketona veidošanās no dvīņu spirta
Tāpēc uzkrāto alkadiēnu hidratācijas reakcijas rezultātā veidojas a ketons.
→ Konjugēts vai aizstājējs alkadiēns
Tas ir alkadiēns, kuram ir divas dubultās saites, vienlaikus iesaistot četras oglekļa atomiem, tas ir, ir viena saite, kas atdala saitēs iesaistītos oglekļus dubultspēles.
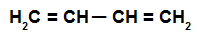
Mainīgā alkadiēna strukturālā formula
Mainīgos alkadiēnos notiek to dubulto saišu rezonanse. Tādējādi pi saites elektroni maina pozīciju (sarkanās bultiņas), kā parādīts šajā diagrammā:
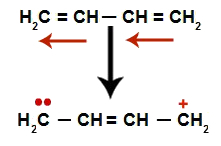
Shematiski attēlota rezonanse mainīgā alkadiēnā
Mums parasti ir dubultās saites izskats tieši starp ogļūdeņražiem, kur iepriekš bija divi dubultnieki, un izveidojot divas saites vietas, pa vienai uz katra oglekļa, kas vairs neveido dubulto saiti (piemērā, ogles 1 un 4). Ķēdes 1. un 4. ogleklis saņem H+ un ak- no ūdens.

Daļēja hidratācija mainīgā alkadiēnā
Pēc rezonanses jaunās dubultās saites pi saite tiek pārtraukta un H+ un ak- tiek pievienoti alkadiēna molekulai. OH pievieno ogleklim, kas ir vistuvāk pirmajai pievienotajai OH grupai, jo tas tiek pakļauts grupas elektroniskai pievilcībai, kas ir vairāk elektronegatīva.

Hidratācijas pārtraukšana mainīgā alkadiēnā
Rezonanses dēļ mēs sakām, ka mainīgajam alkadiēnam tika veikta 1,4 hidratācija, veidojot dialogu.
→ Alkadiēna izolācija
Tas ir alkadiēns, kam ir divas dubultās saites, kas vienlaikus satur vismaz piecus atomus. oglekļa, tas ir, ir vismaz divas atsevišķas saites, kas atdala saitēs iesaistītos oglekļus dubultspēles.

Izolēta alkadiēna strukturālā formula
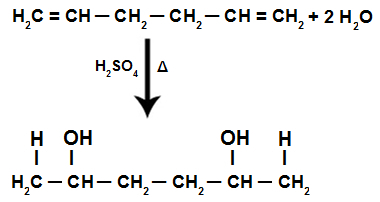
Izolēta alkadiēna hidratācijas reakcijas laikā pi saites tiek sadalītas, kas ir H+ pievieno vairāk hidrogenētiem oglekļiem un OH- pievieno mazāk hidrogenētiem ogļūdeņražiem.

Izolēta alkadiēna hidratācijas reakcijas vienādojums
Tāpēc, pievienojot izolētu alkadiēnu, mums ir tikai diaalkohola veidošanās.
Autors: Diogo Lopes Dias
Avots: Brazīlijas skola - https://brasilescola.uol.com.br/quimica/reacoes-hidratacao-alcadienos.htm
