Organiskās funkcijas grupē oglekļa savienojumus ar līdzīgām īpašībām.
Tā kā pastāv daudzas vielas, kuras veido ogleklis, šī tēma tiek plaši izmantota eksāmenos, lai pārbaudītu zināšanas par organisko ķīmiju.
Domājot par to, mēs pulcējāmies 10 jautājumi Enem un iestājeksāmeni, lai jūs varētu pārbaudīt savas zināšanas par dažādām struktūrām, kas raksturo funkcionālās grupas.
Izmantojiet arī izšķirtspējas komentārus, lai uzzinātu vēl vairāk par šo tēmu.
Ieejas eksāmena jautājumi
1. (UFRGS) Organiskajos savienojumos papildus ogleklim un ūdeņradim skābekļa klātbūtne ir ļoti bieža. Atzīmējiet alternatīvu, kur visi trīs savienojumi satur skābekli.
a) formaldehīds, etiķskābe, etilhlorīds.
b) trinitrotoluols, etanols, fenilamīns.
c) skudrskābe, butanol-2, propanons.
d) izooktāns, metanols, metoksietāns.
e) izobutilacetāts, metilbenzols, heksēns-2.
Pareiza alternatīva: c) skudrskābe, butanols-2, propanons.
Funkcijas, kuru sastāvā ir skābeklis, sauc par skābekļa funkcijām.
Savienojumus, kuru funkcionālajā grupā ir skābeklis, skatīt zemāk.
a) nepareizi. Etilhlorīdam nav skābekļa.
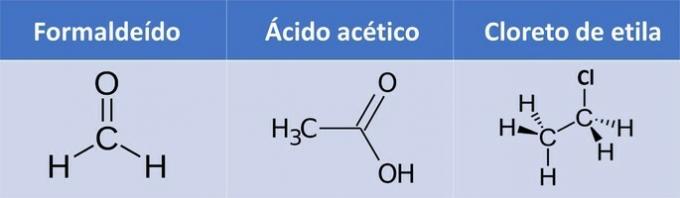
| Savienojums | Organiskā funkcija |
| Formaldehīds | Aldehīds: R-CHO |
| Etiķskābe | Karbonskābe: R-COOH |
| Etilhlorīds |
Alkilhalogenīds: R-X (X apzīmē halogēnu). |
b) nepareizi. Fenilamīnam nav skābekļa.
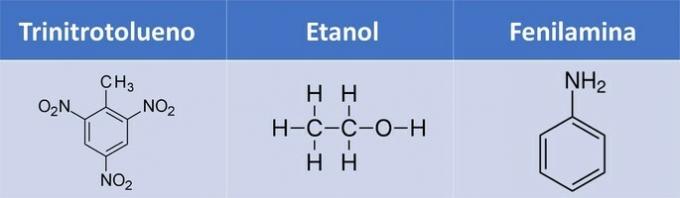
| Savienojums | Organiskā funkcija |
| Trinitrotoluols | Nitrosavienojums: R-NO2 |
| Etanols | Alkohols: R-OH |
| Fenilamīns | Amīns: R-NH2 |
c) PAREIZI. Visiem trim savienojumiem ir skābeklis.
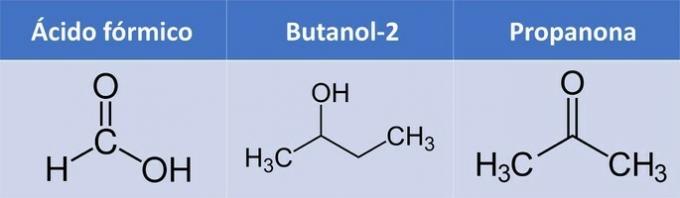
| Savienojums | Organiskā funkcija |
| Skudrskābe | Karbonskābe: R-COOH |
| Butanols-2 | Alkohols: R-OH |
| Propanons | Ketons: R1-KRĀSA2 |
d) nepareizi. Izooktānam nav skābekļa.
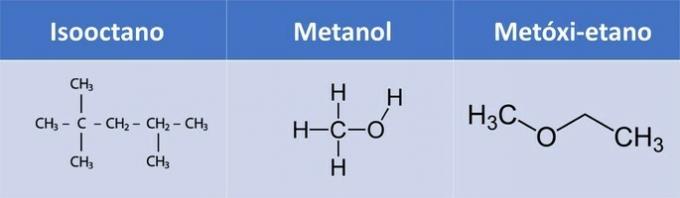
| Savienojums | Organiskā funkcija |
| izooktāns | Alkāns: CNēH2n+2 |
| Metanols | Alkohols: R-OH |
| Metoksi-etāns | Ēteris: R1-O-R2 |
e) nepareizi. Metilbenzolā un heksēn-2 nav skābekļa.
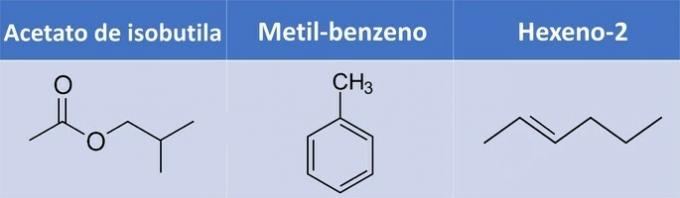
| Savienojums | Organiskā funkcija |
| Izobutilacetāts | Estere: R1-COO-R2 |
| Metilbenzols | Aromātisks ogļūdeņradis |
| Heksēns-2 | Alkēns: CNēH2n |
| A kolonna | B kolonna |
|---|---|
| 1. Benzols |
|
| 2. Etoksietāns |
|
| 3. Etilmetanāts |
|
| 4. Propanons |
|
| 5. metāls |
|
PAREIZA skaitļu secība B slejā no augšas uz leju ir:
a) 2 - 1 - 3 - 5 - 4.
b) 3 - 1 - 2 - 4 - 5.
c) 4 - 3 - 2 - 1 - 5.
d) 3 - 2 - 5 - 1 - 4.
e) 2 - 4 - 5 - 1 - 3.
Pareiza alternatīva: b) 3 - 1 - 2 - 4 - 5.
| ( 3 ) Esteris | 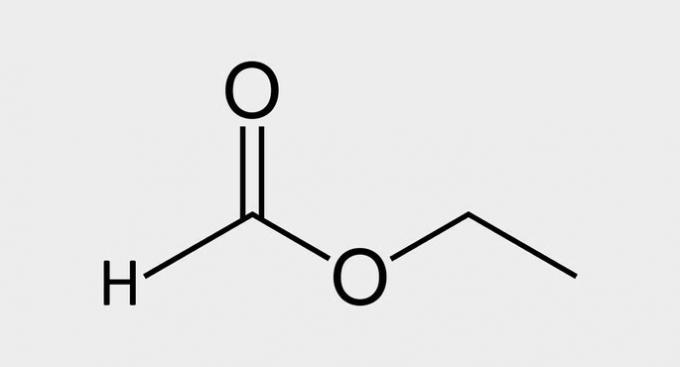 |
| Etilmetanāts |
esteri ir atvasināti no karbonskābēm, kur funkcionālajā grupā -COOH ūdeņradis ir aizvietots ar oglekļa ķēdi.
| ( 1 ) Ogļūdeņradis | 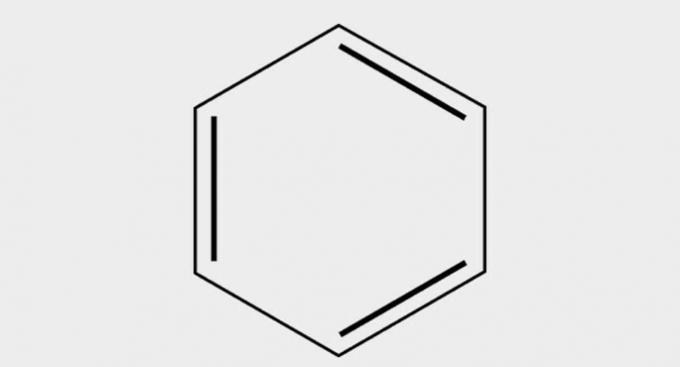 |
| Benzols |
Ogļūdeņraži ir savienojumi, ko veido oglekļa un ūdeņraža atomi.
| ( 2 ) ēteris |  |
| etoksietāns |
ēteri ir savienojumi, kuros skābeklis ir saistīts ar divām oglekļa ķēdēm.
| ( 4 ) Ketons |  |
| Propanons |
Ketoni karbonilgrupa (C = O) ir saistīta ar divām oglekļa ķēdēm.
| ( 5 ) aldehīds | 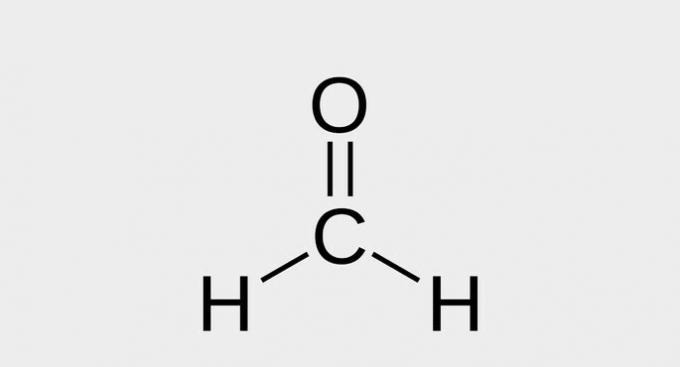 |
| metāls |
Aldehīdi ir savienojumi, kuriem ir funkcionālā grupa -CHO.
a) Pierakstiet četru amīnu strukturālās formulas.
Amini ir savienojumi, kurus teorētiski veidoja no amonjaka (NH3), kurā ūdeņraža atomus aizstāj ar oglekļa ķēdēm.
Saskaņā ar šīm aizstāšanām amīnus iedala:
- Primārais: slāpeklis ir saistīts ar oglekļa ķēdi.
- Sekundārais: slāpeklis saistīts ar divām oglekļa ķēdēm.
- Terciārs: slāpeklis, kas saistīts ar trim oglekļa ķēdēm.
Četri amīni, kuriem ir molekulārā formula C3H9N ir izomēri, jo tiem ir vienāda molekulmasa, bet atšķirīga struktūra.

Uzziniet vairāk vietnē: Manējā un Izomērija.
b) Kuriem no šiem amīniem ir zemāka viršanas temperatūra nekā pārējiem trim? Pamatojiet atbildi struktūras un starpmolekulāro spēku izteiksmē.
Lai gan tiem ir viena un tā pati molekulārā formula, amīniem ir atšķirīga struktūra. Zemāk ir vielas un to viršanas temperatūras.
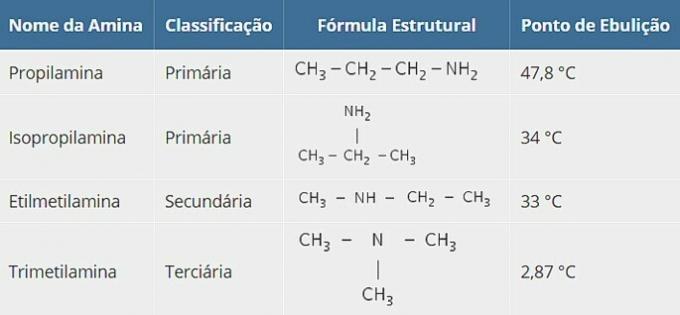
Lai gan tiem ir vienāda molekulārā formula, amīniem ir atšķirīga struktūra, un tas atspoguļo starpmolekulāro spēku veidu, ko šīs vielas pārnēsā.
Ūdeņraža saite vai tilts ir spēcīgas saites tips, kurā ūdeņraža atoms ir saistīts ar elektronegatīvu elementu, piemēram, slāpekli, fluoru vai skābekli.
Elektronegativitātes starpības dēļ tiek izveidota spēcīga saite un trimetilamīns tas ir vienīgais, kam nav šāda veida sakaru.
Skatiet, kā notiek ūdeņraža saites primārajos aminos:
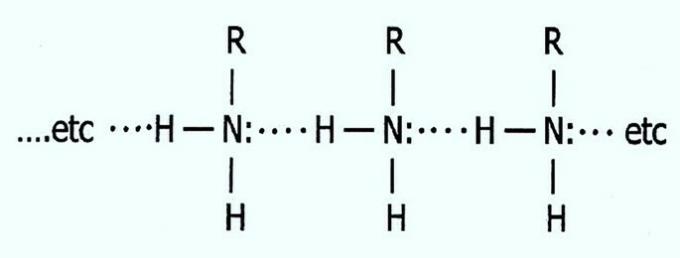
Tāpēc propilamīnam ir visaugstākā viršanas temperatūra. Spēcīga mijiedarbība starp molekulām apgrūtina saišu pārtraukšanu un līdz ar to pāreju gāzveida stāvoklī.
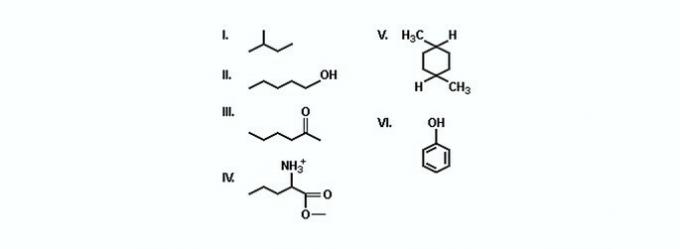
Analizējiet attēlotos savienojumus.
() Divas no tām ir aromātiskas.
() Divi no tiem ir ogļūdeņraži.
() Divi no tiem apzīmē ketonus.
() V savienojums ir dimetilcikloheksāns.
() Vienīgais savienojums, kas veido sāļus, reaģējot ar skābēm vai bāzēm, ir IV.
Pareiza atbilde: F; V; F; V; V.
(FALSE) Divas no tām ir aromātiskas.
Aromātiskiem savienojumiem ir pārmaiņus viena un divas saites. Piedāvātajos savienojumos ir tikai viens aromātisks fenols.
(PATIESA) Divi no tiem ir ogļūdeņraži.
Ogļūdeņraži ir savienojumi, kas sastāv tikai no oglekļa un ūdeņraža.
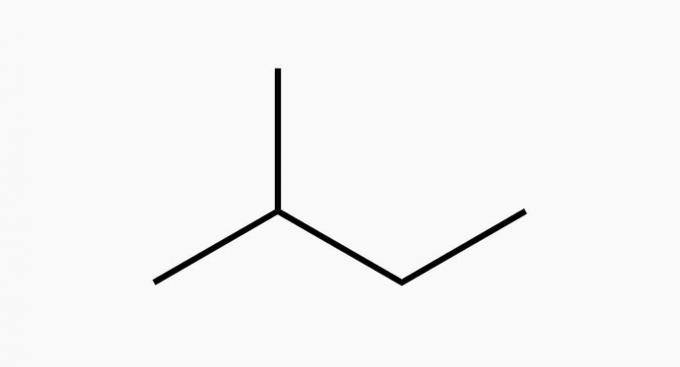
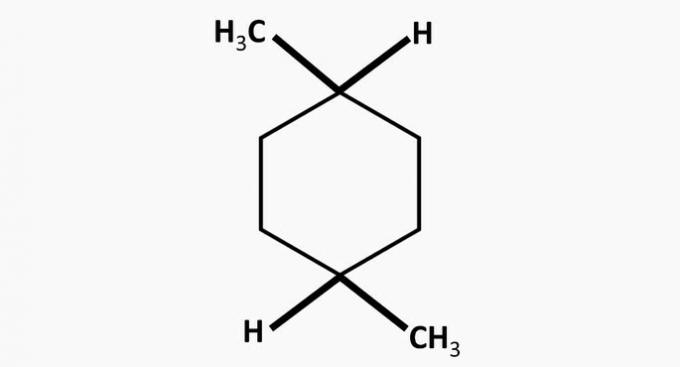
(FALSE) Divi no tiem apzīmē ketonus.
Ketoni ir savienojumi, kuriem ir karbonilgrupa (C = O). Parādītajos savienojumos ir tikai viens ketons.

(PATIESA) Savienojums V ir dimetilcikloheksāns, ciklisks ogļūdeņradis ar diviem metilgrupām.
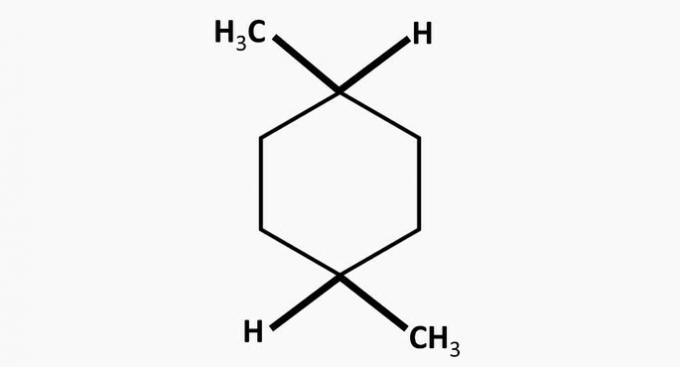
(PATIESA) Vienīgais savienojums, kas veido sāļus, reaģējot ar skābēm vai bāzēm, ir IV.
Savienojums ir esteris, kura funkcionālā grupa ir -COO-.
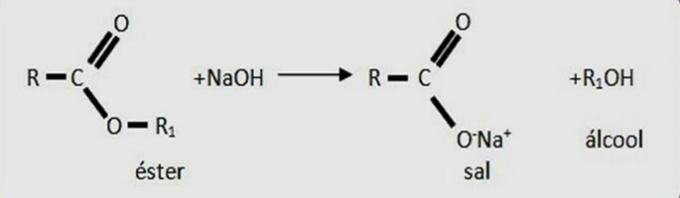
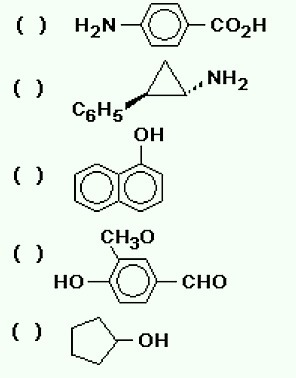
5. (UFRS) Turpmāk uzskaitīti sešu organisko savienojumu ķīmiskie nosaukumi un iekavās to attiecīgie pielietojumi; un vēlāk attēlā - piecu šo savienojumu ķīmiskās formulas. Saistiet tos pareizi.
| Savienojumi | Struktūras |
|---|---|
|
1. p-aminobenzoskābe (izejviela anestēzijas novokaīna sintēzei) |
 |
|
2. ciklopentanols (organiskais šķīdinātājs) | |
|
3. 4-hidroksi-3-metoksibenzaldehīds (mākslīgā vaniļas garša) | |
|
4. (izejviela karbarila insekticīdam) | |
|
5. trans-1-amino-2-fenilciklopropāns (antidepresants) |
Pareizā iekavu aizpildīšanas secība no augšas uz leju ir
a) 1 - 2 - 3 - 4 - 5.
b) 5 - 3 - 1 - 2 - 4.
c) 1 - 4 - 3 - 5 - 2.
d) 1 - 5 - 4 - 3 - 2.
Pareiza alternatīva: d) 1 - 5 - 4 - 3 - 2.
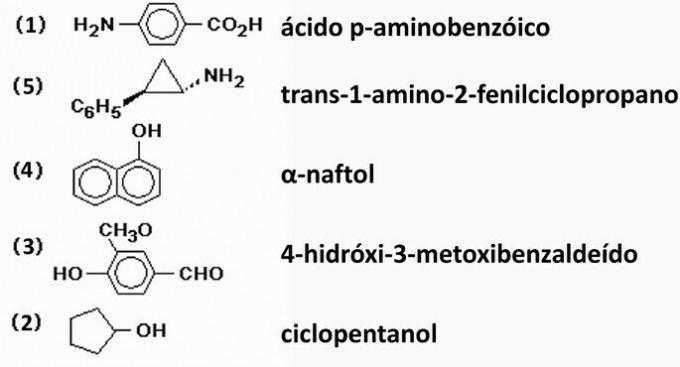
- p-aminobenzoskābe: karbonskābe ar -COOH funkcionālo grupu, kas pievienota aromātiskajam gredzenam ar aminogrupu.
- Trans-1-amino-2-fenilciklopropāns: ciklisks ogļūdeņradis ar diviem zariem: amino un fenilgrupa.
-
-naftols: fenols, ko veido divi aromātiskie gredzeni.
- 4-hidroksi-3-metoksibenzaldehīds: jaukts savienojums, ko veido trīs funkcionālās grupas: aldehīds (CHO), ēteris (-O-) un spirts (OH), kas pievienots aromātiskajam benzola gredzenam.
- Ciklopentanols: spirts, kas veidojas, savienojot hidroksilgrupu (OH) ar ciklisko ķēdi.
Uzziniet vairāk vietnē: oglekļa ķēdes un aromātiskie ogļūdeņraži.
Enem jautājumi
6. (Enem / 2012) Propoliss ir dabīgs produkts, kas pazīstams ar savām pretiekaisuma un ārstnieciskajām īpašībām. Šis materiāls satur vairāk nekā 200 līdz šim identificētus savienojumus. Starp tiem daži ir vienkārši pēc struktūras, piemēram, C6H5CO2CH2CH3, kuras struktūra parādīta zemāk.
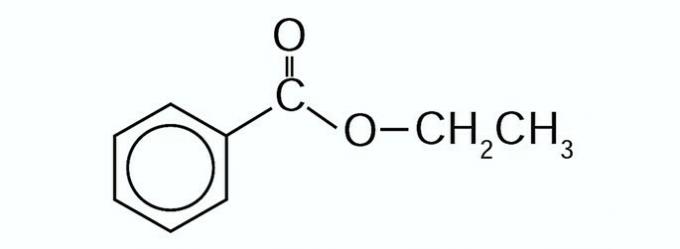
Karboksilskābe un spirts, kas esterifikācijas reakcijas rezultātā spēj ražot attiecīgo esteri, ir attiecīgi:
a) benzoskābe un etanols.
b) propānskābe un heksanols.
c) feniletiķskābe un metanols.
d) propionskābe un cikloheksanols.
e) etiķskābe un benzilspirts.
Pareiza alternatīva: a) benzoskābe un etanols.
a) PAREIZI. Ir etilbenzanoāta veidošanās.
Kad skābe un spirts reaģē esterifikācijas reakcijā, rodas esteris un ūdens.

Ūdens rodas skābes funkcionālās grupas (COOH) hidroksila un spirta funkcionālās grupas (OH) ūdeņraža savienojumā.
Pārējā karbonskābes un spirta oglekļa ķēdes daļa savienojas kopā, veidojot esteri.
b) nepareizi. Ir heksilpropanoāta veidošanās.
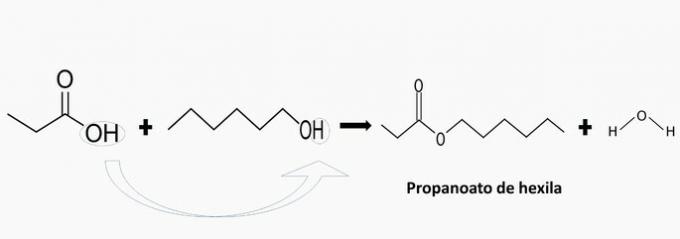
c) nepareizi. Ir metilfenilacetāta veidošanās.
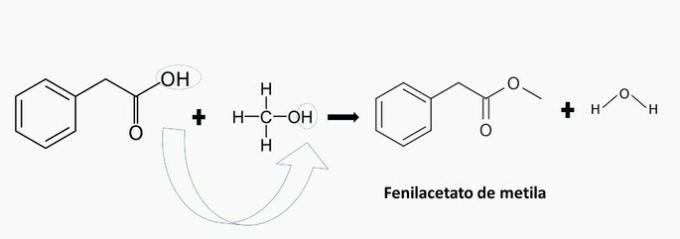
d) nepareizi. Ir cikloheksilpropanoāta veidošanās.
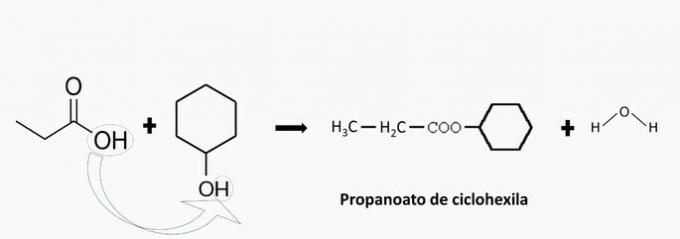
e) nepareizi. Esterifikācijas nav, jo abi savienojumi ir skābi.
Uzziniet vairāk vietnē: karbonskābes un esterifikācija.
7. (Enem / 2014) Jūs esat dzirdējis šo frāzi: starp mums bija ķīmija! Mīlestība bieži ir saistīta ar maģisku vai garīgu parādību, taču mūsu savienojumā ir dažu savienojumu darbība ķermenis, kas rada sajūtas, kad esam tuvu mīļotajam, piemēram, sacīkšu sirds un palielināta frekvence elpošanas. Šīs sajūtas pārraida neirotransmiteri, piemēram, adrenalīns, norepinefrīns, feniletilamīns, dopamīns un serotonīns.

Pieejams: www.brasilescola.com. Piekļuve: 1. martā. 2012. gads (pielāgots).
Minētajiem neirotransmiteriem kopīga ir funkcijas raksturīgā funkcionālā grupa
a) ēteris.
b) alkohols.
c) amīns.
d) ketons.
e) karbonskābe.
Pareiza alternatīva: c) amīns.
a) nepareizi. Ētera funkciju raksturo skābeklis, kas saistīts ar divām oglekļa ķēdēm.
Piemērs:
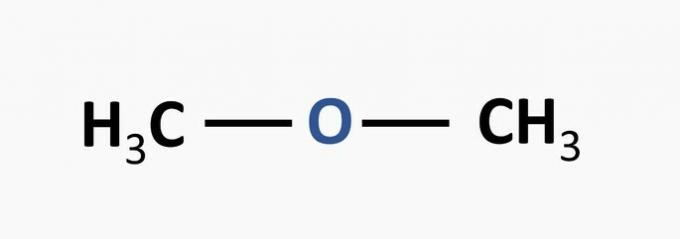
b) nepareizi. Alkohola funkciju raksturo hidroksilgrupa, kas saistīta ar oglekļa ķēdi.
Piemērs:
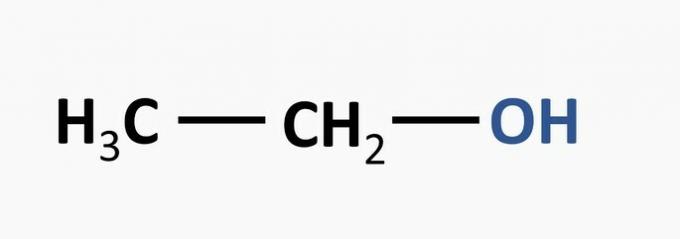
c) PAREIZI. Amīna funkcija tiek novērota visos neirotransmiteros.

Neirotransmiteri ir ķīmiskas vielas, kas darbojas kā biomarķieri, sadalot: biogēnos amīnos, peptīdos un aminoskābēs.
Biogēnie amīni vai monoamīni ir dabisko aminoskābju fermentatīvās dekarboksilēšanas rezultāts un to raksturo slāpekļa klātbūtne, veidojot organisko savienojumu grupu slāpekļa.
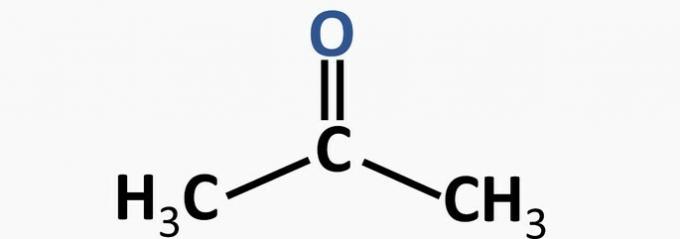
d) nepareizi. Ketona funkciju raksturo karbonila klātbūtne: dubulta saite starp oglekli un ūdeņradi.
Piemērs:
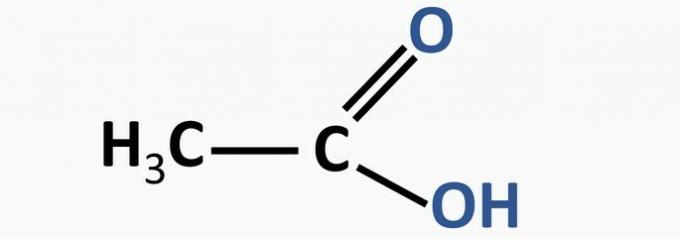
e) nepareizi. Karbonskābes funkciju raksturo -COOH grupas klātbūtne.
Piemērs:
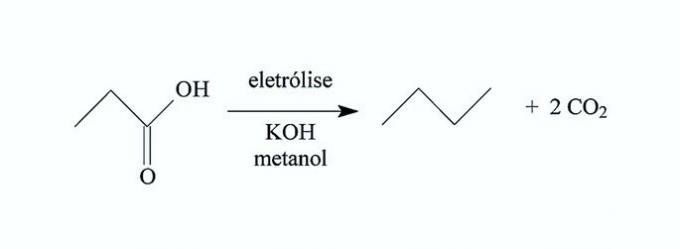
AZEVEDO, D. Ç; GULULART, M. O. F. Stereoselektivitāte elektrodās reakcijās. Jaunā ķīmija, Nr. 2, 1997 (pielāgots).
Pamatojoties uz šo procesu, 3,3-dimetilbutānskābes elektrolīzē iegūtais ogļūdeņradis ir
a) 2,2,7,7-tetrametiloktāns.
b) 3,3,4,4-tetrametilheksāns.
c) 2,2,5,5-tetrametilheksāns.
d) 3,3,6,6-tetrametiloktāns.
e) 2,2,4,4-tetrametilheksāns.
Pareiza alternatīva: c) 2,2,5,5-tetrametilheksāns.
a) nepareizi. Šis ogļūdeņradis rodas 3,3-dimetil-pentānskābes elektrolīzē.
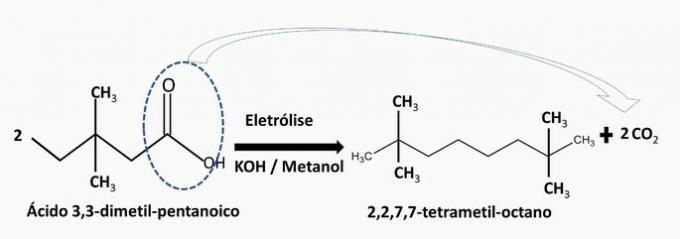
b) nepareizi. Šis ogļūdeņradis rodas 4,4-dimetilbutānskābes elektrolīzē.

c) PAREIZI. 3,3-dimetilbutānskābes elektrolīze rada 2,2,5,5-tetrametilheksānu.

Reakcijā karboksilgrupa tiek atdalīta no oglekļa ķēdes un veidojas oglekļa dioksīds. Elektrolizējot 2 molus skābes, ķēdes apvienojas un veido jaunu savienojumu.
d) nepareizi. Šis ogļūdeņradis rodas 4,4-dimetil-pentānskābes elektrolīzē.

e) nepareizi. Šo ogļūdeņražu nerada anodiska oksidatīvā dekarboksilēšana.
9. (Enem / 2012) Pārtikas ražošanu pasaulē varētu samazināt līdz 40% no pašreizējās, nepiemērojot lauksaimniecības kaitēkļu kontroli. No otras puses, bieža pesticīdu lietošana var izraisīt piesārņojumu augsnē, virszemes un pazemes ūdeņos, atmosfērā un pārtikā. Biopesticīdi, piemēram, piretrīns un koronopilīns, ir bijuši alternatīva, lai samazinātu ekonomisko, sociālo un vides kaitējumu, ko rada pesticīdi.
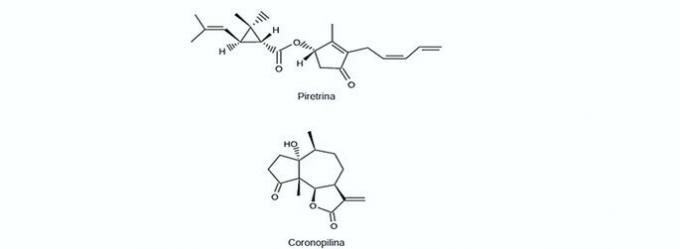
Nosakiet organiskās funkcijas, kas vienlaikus atrodas abu uzrādīto biopesticīdu struktūrā:
a) Ēteris un esteris.
b) ketons un esteris.
c) Alkohols un ketons.
d) Aldehīds un ketons.
e) ēteris un karbonskābe.
Pareiza alternatīva: b) ketons un esteris.
Organiskās funkcijas, kas atrodas alternatīvās, ir:
| karbonskābe | Alkohols |
| Aldehīds | ketons |
| Ēteris | Estere |
Saskaņā ar iepriekš norādītajām funkcionālajām grupām tie, kurus vienlaikus var redzēt abos biopesticīdos, ir ketons un esteris.
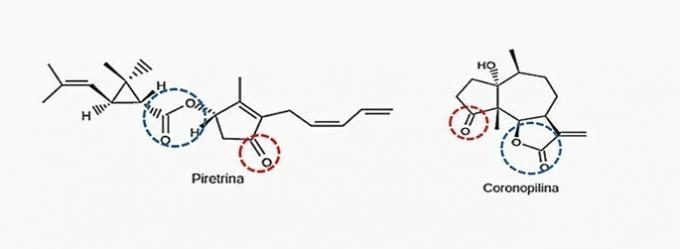
Uzziniet vairāk vietnē: ketons un esteris.
10. (Enem / 2011) Žults ražo aknas, to uzglabā žultspūslī, un tai ir galvenā loma lipīdu gremošanā. Žults sāļi ir steroīdi, kas aknās tiek sintezēti no holesterīna, un to sintēzes ceļš ietver vairākus posmus. Sākot no attēlā attēlotās holskābes, rodas glikohola un taurohola skābes; prefikss glyco- nozīmē aminoskābes glicīna un prefiksa tauro-, aminoskābes taurīna atlikuma klātbūtni.
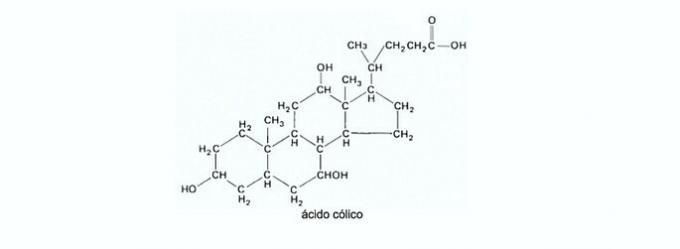
UCKO, D.. Ķīmija veselības zinātnēm: ievads vispārējā, organiskajā un bioloģiskajā ķīmijā. Sanpaulu: Manole, 1992 (pielāgots).
Kombinācija starp holskābi un glicīnu vai taurīnu rada amīda funkciju, kas veidojas, reaģējot starp šo aminoskābju amīnu grupu un grupu
a) holskābes karboksilgrupa.
b) holskābes aldehīds.
c) holskābes hidroksilgrupa.
d) holskābes ketons.
e) holskābes esteris.
Pareiza alternatīva: a) karboksilholskābe.
Šī ir amīda funkcijas vispārīgā formula:
Šo grupu iegūst no karbonskābes kondensācijas reakcijā ar amīnu grupu.
Šajā procesā notiks ūdens molekulas eliminācija saskaņā ar vienādojumu:

Holīnskābē esošais karboksilgrupa (-COOH) spēj reaģēt ar aminogrupu (-NH2) aminoskābes, piemēram, glicīna vai taurīna.

Vairāk vingrinājumu no Organiskā ķīmija, Skatiet arī: Vingrinājumi ogļūdeņražiem.

