Alkēni vai alkēni ir ogļūdeņraži, kuru oglekļa ķēdē ir divkārša saite.
Alkēnu vispārējā formula ir: CNēH2n.
Lielākā daļa alkēnu tiek ražoti laboratorijā, un maz ir dabā.
Iespējas
Alkēnu galvenās īpašības ir:
- bezkrāsains
- Nešķīst ūdenī
- Šķīst spirtā un ēterī
- Tie ir reaktīvāki nekā alkāni
- Kušanas un viršanas temperatūras ir augstākas nekā alkāniem ar tādu pašu oglekļa atomu skaitu
- Vienkāršākais alkēns ir etilēns vai etilēns
Ziniet arī par:
- alkāni
- Alkīni
- alkadiēns
Nomenklatūra
Alkēni saņem tādu pašu nomenklatūru kā citi ogļūdeņraži.
PREFIX + INFIX + SUFFIX
Prefikss norāda ogļu daudzumu galvenajā ķēdē.
Infiksu piešķir termins "en", kas apzīmē dubulto saiti. Piedēklu piešķir burts "o", kas norāda ogļūdeņraža savienojumu.
Tādējādi alkēnus sauc par sufiksu –Eno, kas norāda dubulto saiti.
Turklāt jānorāda dubultās saites pozīcija. Šis skaitlis ir pirms alkēna nosaukuma un norāda oglekļa atomu, kur sākas saikne.
Oglekļa ķēdi sāk numurēt no dubultās saites tuvākā gala.
Piemēri
Etilēns vai etilēns: CH2 = CH2
Propilēns vai propilēns: CH2 = CH - CH3, kura ekvivalenta formula ir uzrakstīta šādi: CH3 - CH = CH2
1-butēns: CH2 = CH - CH2 - CH3
2-butēns: CH3 - CH = CH - CH3
Parasti sastopami arī alkēni izomērija:
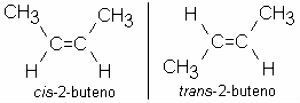
sazaroti alkēni
Alkēnus var arī sazarot. Šajā gadījumā galvenā ķēde ir garākā, un tai ir dubultā saite.
Piemērs:
5-metil-2-heksāns
Uzziniet vairāk par Ogļūdeņražu nomenklatūra.
Papildiniet savu pētījumu par Ogļūdeņraži. Lasiet arī:
- Benzols
- Butāns
- Ciklāni
- Nafta
- Organiskie savienojumi
- Aromātiski ogļūdeņraži
- Vingrinājumi ogļūdeņražiem