Alotropija ir parādība, kas rodas, ja vienam un tam pašam ķīmiskajam elementam ir īpašība veidot vairāk nekā vienu vienkāršu vielu.. Šīs alotropās šķirnes var atšķirties elementa atomu skaita dēļ, kas ir savienoti kopā molekulā, vai atomu izvietojuma dēļ kristāla režģī.
Viens no elementiem, kuriem ir alotropās šķirnes, ir fosfors (P), no kuriem visbiežāk sastopams baltais fosfors tas ir sarkanais fosfors. Šie divi fosfora alotropi atšķiras nevis ar atšķirīgo telpisko izvietojumu, jo abus pamatā veido tetraedriskas molekulas, bet gan fosfora atomu daudzums katrā ir atšķirīgs.
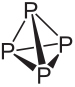
Skatiet baltā un sarkanā fosfora sastāvu un galvenās īpašības:
- Baltais fosfors:
Baltā fosfora molekulārā formula ir P4, kas nozīmē, ka tā molekulas sastāv no četriem fosfora atomiem.

Šis fosfora veids ir ārkārtīgi reaktīvs, lielā mērā pateicoties spriegumam 60 ° leņķī starp tā saitēm. Tas ir tik reaģējošs, ka tas jāuzglabā ūdenī, lai tas nesaskartos ar gaisu un eksplodētu. Rīkojoties ar to, jābūt ļoti uzmanīgam, jo norijot tas izraisa smagus ādas apdegumus un saindēšanos (tikai 0,1 g uzņemtā baltā fosfora var izraisīt nāvi).
Kā redzat zemāk, baltais fosfors ir balta vaska veida cieta viela.

Baltais fosfors tiek uzglabāts ūdenī, lai nesaskartos ar gaisu *
Ja karsē bez gaisa, baltais fosfors pārvēršas par sarkano fosforu.
- sarkanais fosfors:
Sarkanajam fosforam nav noteiktas struktūras, taču ir pierādījumi, ka tas ir makromolekulas, kas veidojas, saistoties minētajām tetraedriskajām struktūrām (P4), ko pārstāv PNē.
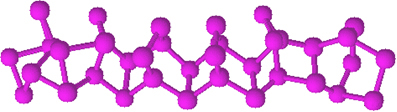
Tas ir daudz mazāk reaktīvs nekā baltais fosfors, tomēr tas var uzliesmot, ja to berzē. Tāpēc to lieto sērkociņu kastīšu sānu virsmās. Kad mēs berzējam zobu bakstāmais uz kastes virsmas, sērkociņš aizdegas un, savukārt, aizdedzina viegli uzliesmojošu materiālu uz zobu bakstāmais galvas.
Dažās valstīs sērkociņš tiek uzlikts uz zobu bakstāļa galvas P formā4s3.
Sarkanais fosfors ir amorfs pulveris, tas ir, tam nav kristāliskas struktūras, un tas ir tumši sarkanā krāsā, kā parādīts zemāk:

Sarkanā fosfora pulveris.
* Attēlu autorība pieder W. Oelen un viņu var atrast šeit.
Autore Jennifer Fogaça
Beidzis ķīmiju
Avots: Brazīlijas skola - https://brasilescola.uol.com.br/quimica/alotropia-fosforo.htm

