Jauda, kas savienojumiem jāpiesaista elektriskiem lādiņiem, tiek definēta kā polaritāte, kurai ir atšķirīgs raksturs atkarībā no savienojuma, kurā tā atrodas.
Kas attiecībā uz jonu un kovalentu saiti būtu polāra vai nepolāra?
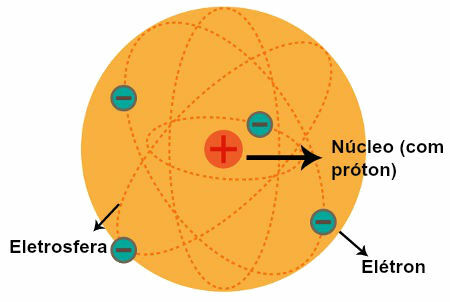
Jonu savienojumi tiek uzlādēti ar elektriskiem lādiņiem: katjoniem un anjoniem, kurus attiecīgi sauc par pozitīvajiem un negatīvajiem poliem. Tos attēlo apzīmējumi δ + un δ-. Jonu vielas reaģē ar citiem savienojumiem šo polu klātbūtnes dēļ, kas padara saiti nestabilu. Piemērs: hlora un nātrija atomu jonu saite rada savienojumu nātrija hlorīds (Na + Cl-), ko tautā sauc par galda sāli.
Īsāk sakot: katra jonu saite ir polārā saite.
Kovalentie savienojumi lielākoties tiek klasificēti kā nepolāri.
Bet atcerieties: tas nenozīmē, ka katrs kovalents savienojums ir nepolārs. Poli ir saistīti ar elektronegativitāti, ja kovalentā saite ir starp vienas un tās pašas elektronegativitātes atomiem, saite būs nepolāra, jo polu neveidojas.
Piemērs: kovalents savienojums C3H8 (Propāns) nav polārs, redzēsim, kāpēc:
H H H
│ │ │
H C ─ C ─ C ─ H
│ │ │
H H H
Ņemiet vērā, ka saikne notiek starp vienādiem elementiem, tāpēc tiem ir vienāda elektronegativitātes skala.
Nepārtrauciet tūlīt... Pēc reklāmas ir vēl vairāk;)
Autore Líria Alves
Beidzis ķīmiju
Brazīlijas skolu komanda
Redzēt vairāk:
Neaizmirstiet par elektronegativitāti
Ziniet, kuri elementi ir vairāk elektronegatīvi
Vispārīgā ķīmija - Ķīmija - Brazīlijas skola
Vai vēlaties atsaukties uz šo tekstu skolas vai akadēmiskajā darbā? Skaties:
SOUZA, Líria Alves de. "Jonu un kovalento saišu polaritāte"; Brazīlijas skola. Pieejams: https://brasilescola.uol.com.br/quimica/polaridade-das-ligacoes-ionica-covalente.htm. Piekļuve 2021. gada 27. jūnijam.