Aizstāšanas (sintēzes) reakcijas ir tādas, kas rodas, kad noteiktā reaģenta grupa maina pozīciju ar cita reaģenta grupu. Visbiežāk tie notiek augstas stabilitātes savienojumos (ar piesātinātām ķēdēm). Bieži vien šīs sintēzes notiek, iesaistot siltumu vai ultravioleto gaismu reakcijas vidē.
Jūs alkāni tie ir organiski savienojumi, kuriem ir tendence veikt aizvietošanas reakcijas, jo tiem ir tikai piesātinātas ķēdes (starp oglekļa atomiem ir tikai vienkāršas saites). Tos plaši izmanto sintēzēm, kuru izcelsme ir organiskie halogenīdi, piemēram, metilhlorīds (gāze, ko lieto kā anestēzijas līdzekli).
Visizplatītākās aizvietošanas reakcijas ar alkāniem ir:
halogenēšana;
nitrēšana;
sulfonēšana;
a) Halogenēšana
Tā ir sintēze, kurā alkāna molekula reaģē ar halogēna molekulu (Cl2, br2, Es2 un F2). I izmantošana2 tas nav tik dzīvotspējīgs, jo veicina ārkārtīgi lēnu reakciju. Jau F lietošana2 tas nav ieteicams, jo tā ir eksplozīva reakcija, kas iznīcina organisko vielu.
Alkānu halogenēšanai ar Br2 vai Cl2 notikt,
nepieciešama gaismas klātbūtne (λ) vai spēcīga apkure. Neatkarīgi no izmantotā halogēna, šīs aizvietošanas reakcijas gala produkts vienmēr būs a organiskais halogenīds. Pēc tam aizvietošana notiks starp alkāna oglekļa un halogēna atomu ūdeņraža atomu, kā rezultātā tiks iegūts organiskais halogenīds un skābes halogenīds (neorganiskā skābe). Skatiet piemēru:
Ja alkānā ir vairāk nekā divi ogļūdeņraži, ūdeņradis tiks aizstāts ar halogēnu saskaņā ar šādu prioritātes secību:
H terciārajā ogleklī> H sekundārajā ogleklī> H primārajā ogleklī
Nākamajā piemērā mēs varam redzēt, ka sekundārā oglekļa H ir aizstāts ar Br atomu.
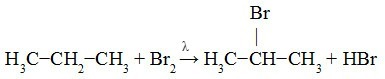
Novērošana: ikreiz, kad alkānā ir vairāk nekā divi ogļi, veidosies vairāk nekā viens organiskais halogenīds. Izveidoto halogenīdu daudzums notiks pēc prioritātes secības. Skatiet dažus piemērus:
Butāna bromēšana:
Zemāk redzamajā vienādojumā mēs novērojam 2-brombutāna veidošanos (lielākā daudzumā, jo tā ir prioritāte sekundārā oglekļa apmaiņas dēļ) un 1-brombutāna (mazākā mērā daudzums).
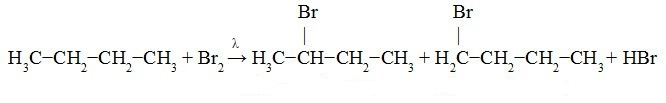
2-brombutāns 1-brombutāns
Metilpropāna hlorēšana:

2-hlor-1-hlor-
2-metil-2-metil-
propāns propāns
Nepārtrauciet tūlīt... Pēc reklāmas ir vēl vairāk;)
b) Nitrēšana
Šajā reakcijā slāpekļskābe (HNO3) reaģē ar alkānu, samainot ūdeņraža alkānu pret nitrogrupu (NO2) skābes, kā rezultātā a nitro savienojums un ūdens molekulā. Tā kā mums ir skābe, nav nepieciešams izmantot katalizatoru.
Novērošana: nitrācijā izmanto tos pašus prioritāros noteikumus, ko izmanto ūdeņraža apmaiņai halogenēšanā.
Izsekot pentāna nitrēšanu:
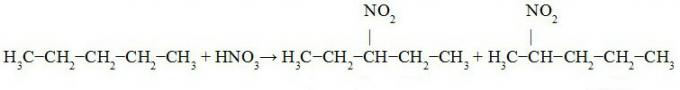
3-nitro-pentāns 2-nitro-pentāns

1-nitropentāns
Iepriekš redzamajā vienādojumā mēs novērojām 3-nitropentāna veidošanos (lielākā daudzumā, jo tā ir prioritāte nomaiņā apmaiņas dēļ jāveic ar terciāro oglekli), 2-nitropentānu (ūdeņraža apmaiņa ar sekundāro oglekli) un 1-nitropentānu (nepilngadīgajā daudzums).
c) Sulfonēšana
Šajā reakcijā sērskābe (H2TIKAI4) reaģē ar alkānu, samainot ūdeņraža alkānu pret sulfongrupu (SO3H) skābes, kā rezultātā rodas a sulfonskābe un ūdens molekula. Tā kā mums ir skābe, nav nepieciešams izmantot katalizatoru.
Novērošana: tie paši prioritārie noteikumi, ko izmanto ūdeņraža apmaiņai halogenēšanā, tiek izmantoti arī sulfonēšanā.
Sliežu ceļa pentāna sulfonēšana:

Penta-3-sulfonskābe Penta-2-sulfonskābe
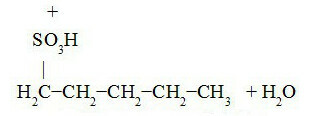
Penta-1-sulfonskābe
Autors: Diogo Lopes Dias
Vai vēlaties atsaukties uz šo tekstu skolas vai akadēmiskajā darbā? Skaties:
DIENAS, Diogo Lopes. "Aizvietošanas reakcijas alkānos"; Brazīlijas skola. Pieejams: https://brasilescola.uol.com.br/quimica/reacoes-substituicao-alcanos.htm. Piekļuve 2021. gada 28. jūnijam.
Ķīmija

Alkāni, ogļūdeņraži, metāns, piesātināta ķēde, alifātiskie, parafīni, degviela, benzīns, minerālvasks, nafta, degslāneklis, dabasgāze, naftas ķīmijas rūpniecība.
Alkānu nomenklatūra, ogļūdeņraža funkcija, oglekļa valences, Starptautiskā Čehijas savienība Tīrā un lietišķā ķīmija, IUPAC, piesātinātie alifātiskie ogļūdeņraži, atsevišķās saites, savienojumi Organisks.
Ķīmija

Noklikšķiniet šeit un uzziniet vairāk par aizvietošanas reakciju - ķīmisko procesu, kurā izmantotie reaģenti (organiskie un neorganiskie) savstarpēji apmainās ar vienu no tā sastāvdaļām, veidojot jaunas vielas. Starp vielām, ko visbiežāk izmanto kā reaģentus, ir alkāni, benzols un organiskie halogenīdi.


