O Tomsona atomu modelis 1898. gadā ierosināja angļu fiziķis Džozefs Džons Tomsons vai vienkārši Dž. Dž. Tomsons. Pēc tam, kad ir vairāki eksperimentāli pierādījumi par elektrona esamību, viņš apgāza piedāvāto atoma nedalāmības teoriju Džons Daltons.
Tomsons, pamatojoties uz savu modeli, apstiprināja un pierādīja elektroni (daļiņas ar negatīvu elektrisko lādiņu) atomā, tas ir, atomam ir subatomiskās daļiņas.
Prāta karte: Thomson Atomic Model
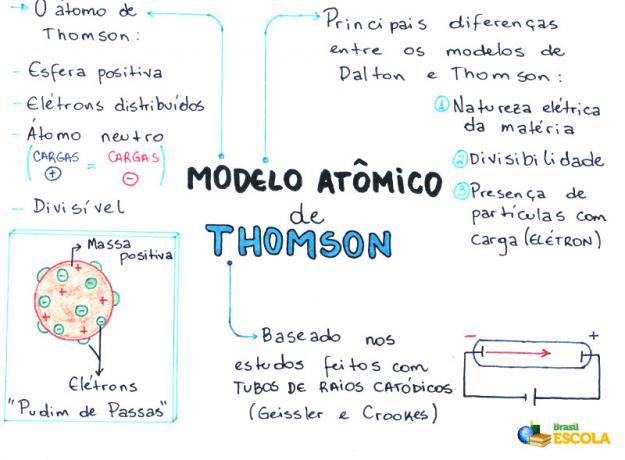
* Lai lejupielādētu domu karti PDF formātā, Noklikšķiniet šeit!
Tomsons piedāvāja savu atomu modeli pamatojoties uz atklājumiem, kas saistīti ar radioaktivitāti, un eksperimentiem, kas veikti ar zinātnieku Geissler un Crookes izveidoto katodstaru lampu. Skatīt šīs caurules attēlojumu:
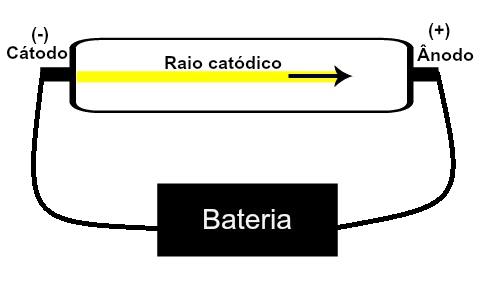
Kad retināta, zema spiediena gāze tiek pakļauta augstam elektriskajam spriegumam (piemēram, 15000 V), tā rada a gaismas kūlis (sastāv no elektriskiem lādiņiem) no katoda (negatīvā pola) virzienā uz anodu (polu pozitīvs).
Ar šo eksperimentu Tomsons nonāca pie secinājuma, ka tad, kad iekšpusē ir gāzveida materiāla atomi no caurules tika pakļauti augstspriegumam, to elektroni tika izvilkti un novirzīti uz plāksni pozitīvs.
Apsvērumi, ko piedāvā Tomsona atomu modelis
Veicot eksperimentus ar katodstaru lampu, Tomsons ierosināja interpretēt, kāds būtu atoms un tā uzbūve. Tātad, pēc viņa teiktā:
- Atoms ir sfēra, bet ne masīva, kā to ierosināja Džona Daltona atomu modelis;
- Atoms ir neitrāls, jo visa matērija ir neitrāla;
- Tā kā atomam ir elektroni, kuriem ir negatīvi lādiņi, tam jābūt pozitīvām daļiņām, lai galīgais lādiņš būtu nulle;
- Elektroni nav fiksēti vai ieslodzīti atomā, tos noteiktos apstākļos var pārnest uz citu atomu;
- Atomu var uzskatīt par nepārtrauktu šķidrumu ar pozitīviem lādiņiem, kur izplatītos elektroni, kuriem ir negatīvs lādiņš;
- saistīja jūsu modeli rozīņu pudiņam (kas attēlo elektronus);
- Tā kā izkliedētajiem elektroniem ir vienāds lādiņš, starp tiem pastāv savstarpēja atgrūšanās, kas padara tos vienmērīgi sadalītus sfērā.
Jaunumi, kurus atomam ierosināja Tomsona modelis
Otrais atomam tika ierosināts Tomsona atomu modelis. Pirmo modeli formulēja Džons Daltons.
Nepārtrauciet tūlīt... Pēc reklāmas ir vairāk;)
Tomsona modelis attiecās uz jaunām zināšanām par atomu, kuras līdz šim nebija ierosinātas zinātniska pamata trūkuma dēļ, piemēram:
- Matērijas elektriskais raksturs;
- Atomu sadalīšana;
- Mazu, uzlādētu daļiņu klātbūtne atomā.
Tomsona atomam norādītās problēmas
Vairāki fiziķi priekšlikuma iesniegšanas laikā Tomsona atomu modelis, pamatojoties uz klasiskās fizikas teorijām, norādīja uz dažām neatbilstībām, kas pastāv šajā modelī:
- Tomsons ierosināja, ka atomam ir stabilitāte attiecībā pret vienmērīgu elektronu sadalījumu, ko var modificēt enerģijas ietekmē. Tomēr klasiskā fizika, kuras pamatā ir elektromagnētisms, neļauj pastāvēt stabilai sistēmai, kuras pamatā ir tikai atgrūšana starp viena lādiņa daļiņām;
- Tomsonam elektroni ir vienmērīgi sadalīti atomā, taču tiem ir iespēja paātrinātā veidā, un tāpēc tai noteiktās frekvencēs jāizstaro elektromagnētiskais starojums specifiski. Tomēr tas netika ievērots.
- Tomsona modelis bieži bija neefektīvs, izskaidrojot atomu īpašības, piemēram, to sastāvu un organizāciju.
* Viktora Rikardo Ferreiras domu karte
Ķīmijas skolotājs
Autors: Diogo Lopes Dias
Vai vēlaties atsaukties uz šo tekstu skolas vai akadēmiskajā darbā? Skaties:
DIENAS, Diogo Lopes. "Thomson's Atomic Model"; Brazīlijas skola. Pieejams: https://brasilescola.uol.com.br/quimica/o-atomo-thomson.htm. Piekļuve 2021. gada 27. jūnijam.
Ķīmija

Nils Bohrs, Bora atoms, atomu fizika, stabils atoms, atomu modelis, planētu sistēma, elektrosfēras slāņi, enerģijas līmeņi, elektronu čaulas, elektronu enerģija, Rezerfordas atomu modelis, ierosinātā stāvokļa atoms.
Ķīmija
Atomi un Visuma uzbūve, atomu teorija, ka viss ir izgatavots, matērija sastāv no atomiem, četru elementu teorija, senie alķīmiķi, atomu teorija, fundamentālā daļiņa.