Gāze un tvaiks
Starpību starp gāzi un tvaiku izsaka no kritiskās temperatūras. Tvaiks ir viela gāzveida stāvoklī, stāvoklī, kuru var sašķidrināt ar pieaugošu spiedienu. Gāze nav vienāda. Tas ir šķidrums, kuru nevar sašķidrināt, vienkārši palielinot spiedienu. Tas padara gāzi atšķirīgu no tvaika.
Gāzu uzvedība
Konkrēta viela gāzveida stāvoklī ir gāze, ja tās temperatūra ir augstāka par kritisko temperatūru, ja temperatūra ir vienāda vai zemāka par kritisko temperatūru, kurā viela ir tvaiks.
Īstajām gāzēm, kuras mēs parasti zinām, piemēram, hēlijam, slāpeklim un skābeklim, katrai no tām ir atšķirīgas un īpašas molekulārās īpašības. Tomēr, ja mēs tos visus ievietojam augstā temperatūrā un zemā spiedienā, viņiem sāk parādīties ļoti līdzīga izturēšanās. Pētot gāzes, tiek pieņemts vienkāršs teorētiskais modelis, kura praksē nepastāv, ar tādu pašu uzvedību kā reālajām gāzēm. Šī tuvināšana kļūst labāka, jo zemāks spiediens un augstāka temperatūra. Šo gāzes modeli sauc ideāla gāze.
Ap 17. un 19. gadsimtu trīs zinātnieki (Žaks Čārlzs, Luijs Dž. Gay-Lussac un Paul E. Clayperon), izpētījis gāzu uzvedību, izstrādāja likumus, kas regulēja perfektu gāzu uzvedību, sauktas arī par ideālām gāzēm. Viņu noteiktie likumi nosaka ideālas gāzes “ārējās” uzvedības noteikumus, kas noved pie tajā tiek skaitīti tikai ar tiem saistītie fiziskie lielumi, kas ir: tilpums, temperatūra un spiediens.
Perfektu gāzu vispārējais likums
Izteicienu, kas nosaka ideālu gāzu vispārējo likumu, var redzēt šādi:
Nepārtrauciet tūlīt... Pēc reklāmas ir vairāk;)
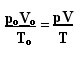
kur lppO, VO un T.O tie ir attiecīgi sākotnējais spiediens, sākotnējais tilpums un sākotnējā temperatūra. Šī ir izteiksme, ko lieto, ja mainās gāzes mainīgie.
Boila likums
Roberts Boils, fiziķis un ķīmiķis, bija tas, kurš noteica likumu, kas regulē gāzes pārveidojumus, kad tās temperatūra tiek turēta nemainīga. Viņa likums saka, ka tad, kad gāze izotermiski pārveidojas, tās spiediens ir apgriezti proporcionāls aizņemtajam tilpumam. No šī likuma mēs to iegūstam kā TO = T Mums vajag:
POVO = pV
Čārlza likums
Čārlza likums ir likums, kas regulē perfektas gāzes pārveidojumus nemainīgā tilpumā. Šīs transformācijas sauc par izohoriskām vai izometriskām transformācijām. Saskaņā ar šo likumu, kad perfektai gāzes masai notiek izohoriska transformācija, tās spiediens ir tieši proporcionāls absolūtai temperatūrai. Matemātiski šo likumu var izteikt šādi:

kur lppO un T.O ir attiecīgi sākotnējais spiediens un sākotnējā temperatūra.
Geja-Lusaka likums
Gay-Lussac likums ir likums, kas regulē perfektas gāzes pārveidojumus pastāvīgā spiedienā. Šo likumu, neraugoties uz Gay-Lussac vārdu, jau bija atklājis fiziķis un ķīmiķis A. C. Charles. Saskaņā ar likumu, kad gāzei notiek izobāriska transformācija, gāzes tilpums ir tieši proporcionāls tās absolūtajai temperatūrai. Matemātiski šo likumu var izteikt šādi:

Kur VO un T.O attiecīgi atbilst sākotnējam tilpumam un sākotnējai temperatūrai.
Autors Marko Aurēlio da Silva
Redzēt vairāk!!
Gāzes pārveidojumi
Zināt, kas ir gāzes transformācijas.
Vai vēlaties atsaukties uz šo tekstu skolas vai akadēmiskajā darbā? Skaties:
SANTOS, Marko Aurēlio da Silva. "Gāzu izpēte"; Brazīlijas skola. Pieejams: https://brasilescola.uol.com.br/fisica/estudo-dos-gases.htm. Piekļuve 2021. gada 27. jūnijam.


