Pakļaujot dažādus elementus liesmas darbībai, mēs pamanām, ka katrs no tiem izstaro atšķirīgu krāsu. Piemēram, ja mēs sadedzinām stronciju, nātrija un vara sāli, mēs attiecīgi redzēsim sarkanas, intensīvi dzeltenas un zaļas krāsas, kā parādīts nākamajā attēlā:

Ja gaisma no šīm liesmām nokrīt uz prizmu, a pārtrauktais spektrs, tas ir, tiks novērotas tikai dažas krāsainas spilgtas līnijas, kas mijas ar reģioniem bez gaismas. Katram elementam mums būs atšķirīgs spektrs.

Šāda veida spektrus sauc emisijas spektrs, jo tos ir izdevis noteikts elements, un tie kalpo tā identificēšanai.
Šādus spektrus ir iespējams iegūt, izmantojot gaismas staru, ko rada elektriskās izlādes caurule augstā stāvoklī temperatūra un zems spiediens, kas satur gāzes no noteiktiem elementiem, piemēram, ūdeņradi, vai kā cēlgāzes zemāk:

Izlaižot šo elektromagnētisko starojumu (gaismu), kas rodas caur prizmu, iegūst katra no šiem elementiem emisijas spektrus.
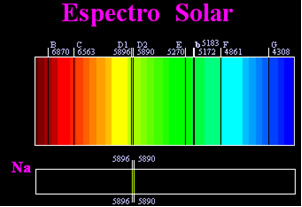
Iepriekš tika uzskatīts, ka sasniegtais saules spektrs ir pilnīgi nepārtraukts, taču angļu zinātnieks Viljams Haids Volastons atklāja, ka līdz strādājot ar ļoti šauru gaismas staru, ar aptuveni 0,01 mm spraugu, varēja redzēt, ka Saules spektrā bija septiņas melnas līnijas par to. Vēlāk jaunie
Džozefs Fraunhofers (1787-1826), izmantojot prizmas un difrakcijas režģus, atklāja, ka Saules spektrs faktiski satur tūkstošiem pārklātu melnu līniju.Kādu laiku vēlāk fiziskā Gustavs Roberts Kirhofs viņš pamanīja, ka dzeltenie plankumi, kas iegūti ar nātrija spektru, atrodas tieši tajā pašā vietā kā divas melnās līnijas Saules spektrā. viņš un ķīmiķis Roberts Vilhelms Bunsens veica vairākus eksperimentus un pamanīja, ka, ja baltā gaisma no Bunsen degļa, piemēram, saules gaisma, iet garām nātrija izstarotajai dzeltenajai gaismai, un spektra radīšanai tiek šķērsota prizma; rezultāts būtu nepārtraukts Saules spektrs varavīksnes krāsās, bet ar melnajām līnijām (ko Fraunhofers sauc par D līnijām) tādā pašā stāvoklī kā dzeltenās līnijas nātrija spektrā.
Nepārtrauciet tūlīt... Pēc reklāmas ir vairāk;)
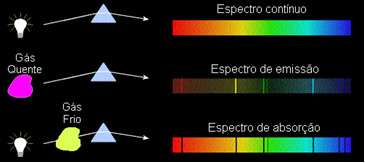
Saule izstaro visu krāsu gaismu, sākot no sarkanās līdz violetai, tomēr, ejot cauri Zemes atmosfērai, esošās gāzes absorbē Saules gaismu tieši to izstarotajās krāsās.
Šāda veida spektrus sauc absorbcijas spektri.
Pamatojoties uz šiem novērojumiem, Kirchoff izveidoja trīs likumiem spektroskopijai, kas ir:
1) Ķermenis necaurspīdīgs karsts jebkurā no trim fizikālajiem stāvokļiem izstaro spektru nepārtraukts.
2) gāze caurspīdīgs - tāpat kā cēlās gāzes, kuras mēs redzējām iepriekš, rada a emisijas spektrs, ar izskatu līnijas spilgti. Šo līniju skaitu un atrašanās vietu noteiks gāzē esošie ķīmiskie elementi.
3) Ja a nepārtraukta spektra šķērso gāzi zemākajā temperatūrā aukstā gāze izraisa tumšās līnijas, tas ir, a absorbcijas spektrs. Tas notika ar saules gaismas spektru, kas iet caur nātrija gāzi. Šajā gadījumā līniju skaits un izvietojums absorbcijas spektrā ir atkarīgs arī no gāzē esošajiem ķīmiskajiem elementiem.
Autore Jennifer Fogaça
Beidzis ķīmiju
Vai vēlaties atsaukties uz šo tekstu skolas vai akadēmiskajā darbā? Skaties:
FOGAÇA, Jennifer Rocha Vargas. "Emisijas un absorbcijas spektri un Kirhofa likumi"; Brazīlijas skola. Pieejams: https://brasilescola.uol.com.br/quimica/espectros-emissao-absorcao-leis-kirchhoff.htm. Piekļuve 2021. gada 27. jūnijam.