Apsveriet šādu ķīmisko līdzsvaru nemainīgā temperatūrā:
3 stundas2. punkta g) apakšpunkts + N2. punkta g) apakšpunkts ↔ 2 NH3. punkta g) apakšpunkts
Pēc Gay-Lussac domām, gāzveida dalībnieku tilpuma daļa reakcijā ir vienāda ar attiecīgo stehiometrisko koeficientu attiecību. Vienkārši sakot, mēs varam teikt, ka reaģentos un produktos esošo molekulu skaits ir vienāds ar koeficientiem vienādojumā.
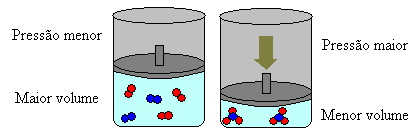
Iepriekš minētajā gadījumā reaģentos mums ir 4 molekulas, bet produktos - 2 molekulas, kas nozīmē, ka reaģentu tilpums ir lielāks un produktu mazāks.
Ja mēs palielināsim spiedienu šajā sistēmā, līdzsvars mainīsies uz mazāku tilpumu, lai samazinātu šo spiedienu. Reakcijas gadījumā, kuru mēs apsveram, pārvietojums notiks tiešā produkta veidošanās virzienā (NH3. punkta g) apakšpunkts).
Tomēr, ja mēs samazinām spiedienu, reakcija virzīsies uz lielāko reaģentu veidošanās tilpumu, kas ir pretējs virzienā (3 H2. punkta g) apakšpunkts + N2. punkta g) apakšpunkts).
Nepārtrauciet tūlīt... Pēc reklāmas ir vairāk;)
Tas notiek saskaņā ar Le Chatelier principu, kurā teikts, ka jebkādi traucējumi (piemēram, spiediena samazināšana vai palielināšana) izraisīja līdzsvara sistēmā liks tai virzīties virzienā, kas samazina šo traucējumu, pielāgojot sevi jaunam līdzsvars.
Īsumā, spiediena izmaiņu ietekmes uz ķīmisko līdzsvaru gadījumā mēs varam teikt sekojošo:
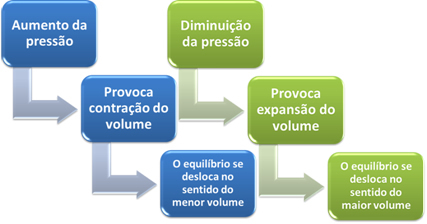
Reakciju gadījumā, kad reaģentu tilpums ir vienāds ar produktu tilpumu, ķīmiskais līdzsvars nemainās.
Autore Jennifer Fogaça
Beidzis ķīmiju
Vai vēlaties atsaukties uz šo tekstu skolas vai akadēmiskajā darbā? Skaties:
FOGAÇA, Jennifer Rocha Vargas. "Spiediena izmaiņas un ķīmiskā līdzsvara pārvietošana"; Brazīlijas skola. Pieejams: https://brasilescola.uol.com.br/quimica/variacao-pressao-deslocamento-equilibrio-quimico.htm. Piekļuve 2021. gada 28. jūnijam.
Ķīmija

Pārbaudiet savas zināšanas un uzziniet vairāk, izmantojot šo atrisināto vingrinājumu sarakstu par ķīmisko līdzsvaru. Izmantojot šo materiālu, jūs varēsiet labāk saprast, kā darboties līdzsvara konstantēm (Kp, Kc un Ki), līdzsvara nobīdei, pH un pOH, kā arī līdzsvaram tā sauktajos buferšķīdumos.



