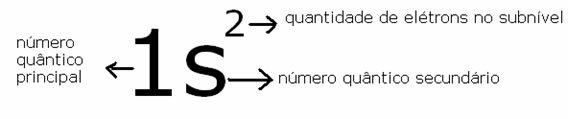
Alotropija ir īpašība, ka dažiem ķīmiskiem elementiem ir jāveido dažādas vienkāršas vielas, tas ir, vielas, kuras veido tikai viena veida elementi.
Tiek sauktas dažādas izveidojušās vielas formas vai alotropās šķirnes vai no alotropi.
Šie alotropi var atšķirties divu galveno iemeslu dēļ:
1. Tās garīgums: molekulu veidojošo atomu skaits;
2. Struktūra: Katrai alotropiskajai formai atomu izvietojums kristāla režģī ir atšķirīgs.
Sērs (S) ir elements, kuram ir visplašākās alotropās formas, ieskaitot molekulas no S2, S4, S6un s8, kas atšķiras ar atomu skaitu katrā molekulā. Visus šos sēra alotropus var atrast vietās, kur ir tendence uz vulkāna izvirdumiem, starp temperatūru 444,6 ° C un 1000 ° C. Tomēr virs 1000 ° C S2 sāk sadalīties atomu sērā (S0).
Tomēr vissvarīgākie sēra alotropi ir divi: o rombveida sērs tas ir monoklīniskais sērs.
Abus veido viena molekulārā formula, s8, atšķirība starp abām būtnēm kristālu režģī esošo atomu telpiskajā izvietojumā.

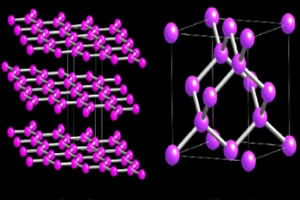
Kā redzat attēlā zemāk, rombveida sērs ir dzeltenu un caurspīdīgu kristālu formā, bet monoklīniskais ir adatas formas un necaurspīdīgs:

Nepārtrauciet tūlīt... Pēc reklāmas ir vairāk;)
Starp šīm divām sēra alotropajām formām rombisks ir visizplatītākais. Tā blīvums ir vienāds ar 2,07 g / cm3 pie 20 ° C, kušanas temperatūra ir vienāda ar 112,8 ° C un viršanas temperatūra ir vienāda ar 444,6 ° C.
Monoklīnikas blīvums ir 1,96 g / cm3 pie 20 ° C kušanas temperatūra ir vienāda ar 119 ° C un tāda pati viršanas temperatūra kā rombveida sērs. Apkārtējos apstākļos abi ir dzeltens pulveris bez smaržas, nešķīst ūdenī un ļoti labi šķīst oglekļa sulfīdā (CS2).

Sēram ir vairākas rūpnieciskas izmantošanas iespējas, galvenokārt sērskābes H ražošanā2TIKAI4, kas, savukārt, tiek plaši izmantota dažādu produktu ražošanā. Sērskābes patēriņš ekonomiskās nozīmes dēļ bieži var norādīt uz valsts attīstības pakāpi.
Vēl viens svarīgs sēra pielietojums ir gumijas vulkanizācija, kas ir 2 līdz 30% sēra pievienošana gumijai, karsējot un katalizatoru klātbūtnē, veidojot trīsdimensiju polimēru ar sēru, kas kalpo kā tilts starp ķēdēm oglekļa. Tas padara dabisko kaučuku izturīgāku un elastīgāku, gatavu dažādiem lietojumiem, piemēram, riepu izgatavošanai.
Sēru izmanto arī melnā pulvera, insekticīdu, kosmētikas un farmaceitisko līdzekļu ražošanā, piemēram, antibiotikas, kuru pamatā ir sulfāts.
* Attēla redakcijas kredīti: emran / Shutterstock.com
Autore Jennifer Fogaça
Beidzis ķīmiju
Vai vēlaties atsaukties uz šo tekstu skolas vai akadēmiskajā darbā? Skaties:
FOGAÇA, Jennifer Rocha Vargas. "Sēra alotropija"; Brazīlijas skola. Pieejams: https://brasilescola.uol.com.br/quimica/alotropia-enxofre.htm. Piekļuve 2021. gada 28. jūnijam.
Ķīmija
Kas ir alotropija, vienkāršas vielas, gāzes skābeklis, ozons, alotropiskās formas, ķīmiskais elements skābeklis, ultravioletie saules stari, dimants, grafīts, atoms, baltais fosfors.