O aprēķinot atomu daļiņu skaitu lieto, lai norādītu protonu (kodolā), elektronu (elektrosfērā) un neitronu (kodolā) daudzumu, kas atrodas jebkurā atomā vai jonā. Lai to izdarītu, ir svarīgi zināt dažas atomu īpašības:
1- Atomu skaitlis (Z)
Tas ir matemātisks kods, ko attēlo lielais burts Z un kas atrodas atoma saīsinājuma apakšējā kreisajā pusē:
ZX
Tas norāda protonu skaitu (p) kodolā un elektronu (e) skaitu atoma elektrosfērā. Tātad vispārīgi:
Z = p = e
2- Masas numurs (A)
Tas ir matemātisks kods, kas atbilst jebkura atoma kodolā esošo protonu (p) un neitronu (n) skaita summai. Vienādojumu, kas apzīmē masas skaitli, izsaka šādi:
A = p + n
Tā kā protonu skaits ir vienāds ar atomu skaitli, masas skaitļa aprēķināšanai mēs varam uzrakstīt vienādojumu šādi:
A = Z + n
Ja mēs zinām atoma masas un atomu skaitu, neitronu skaitu varam noteikt šādi:
n = A - Z
3- joni
Tie ir atomi, kas zaudē vai iegūst elektronus. Viņiem ir pozitīva vai negatīva zīme, kas novietota attēlojuma augšējā labajā stūrī, kā parādīts šajā modelī:
X+ vai X-
Pozitīvais jons: To sauc par katjonu, un pozitīvā zīme norāda, ka tas ir zaudējis elektronus.
Negatīvs jons: To sauc par anjonu, un negatīvā zīme norāda, ka tas ir ieguvis elektronus.
Nepārtrauciet tūlīt... Pēc reklāmas ir vairāk;)
4- Atomu līdzības
a) Izotopi
Atomi, kuriem ir vienāds atomu skaitlis un dažādi masas numuri. Piemērs:
7X14 un 7Jā16
Atomiem X un Y ir vienāds atomu skaitlis (pa kreisi no akronīma), tas ir, vienāds ar 7. Atoma X masas numurs (akronīma labajā pusē) ir vienāds ar 14, un atoma Y masas skaitlis ir 16.
b) Izobāri
Atomi, kuriem ir vienāds masas skaitlis un dažādi atomu skaitļi. Piemērs:
15X31 un 13Jā31
Atomu X un Y masas numurs (pa labi no akronīma) ir vienāds ar 31. Savukārt Atom X atoma skaitlis ir vienāds ar 15, bet atomam Y ir 13.
c) Izotoni
Atomi, kuriem ir atšķirīgi masas un atomu skaitļi, bet vienāds neitronu skaits.
d) izoelektronika
Atomi, kuriem ir vienāds elektronu skaits. Piemērs:
12X+2 un 7Jā-3
Atomam X ir atomu skaitlis, kas vienāds ar 12, un tas ir katjons (ar pozitīvu lādiņu +2), tāpēc tas zaudē divus elektronus, tādējādi tā elektrosfērā ir 10 elektroni. Savukārt atomam Y ir atomu skaitlis, kas vienāds ar 7, un tas ir anjons (ar negatīvu lādiņu -3), tāpēc tas iegūst trīs elektronus, tādējādi tā elektrosfērā ir 10 elektroni.
Prāta karte: Atomu daļiņas
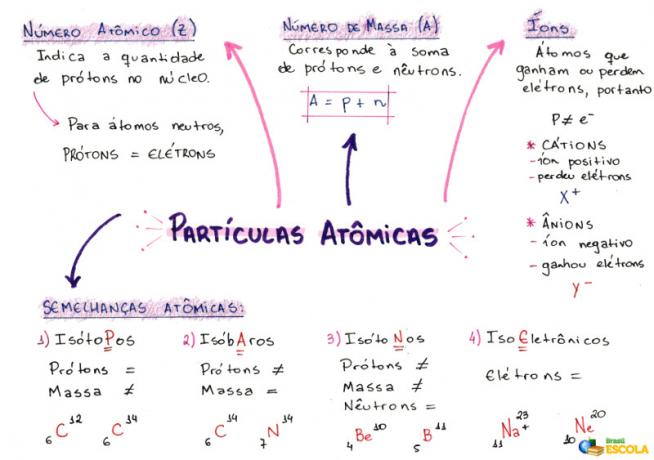
* Lai lejupielādētu domu karti PDF formātā, Noklikšķiniet šeit!
Atomu daļiņu skaita aprēķināšanas piemēri
1. piemērs: Nosaka protonu, neitronu un elektronu skaitu atomā 14X29.
Tika norādītas šādas vērtības atomam X:
Masas numurs (augšējā labajā stūrī) = 29
Atomu skaitlis (apakšā pa kreisi) = 14
Lai noteiktu protonu skaitu:
Protonu skaits vienmēr ir vienāds ar atomu skaitli, tāpēc X atomā ir 14 protoni.
Lai noteiktu elektronu skaitu:
Tā kā atoms X nav jons, tāpēc elektronu skaits ir vienāds ar protonu skaitu, tas ir, 14.
Lai noteiktu neitronu skaitu:
Neitronu skaitu nosaka, izmantojot masas un protonu skaitu šādā formulā:
A = p + n
29 = 14 + n
29 - 14 = n
n = 15
2. piemērs: Nosakiet jonu X protonu, neitronu un elektronu skaitu+3, zinot, ka to masas un atomu skaits ir attiecīgi 51 un 23.
Tika norādītas šādas jonu X vērtības:
Masas numurs = 51
Atomu skaitlis (apakšā pa kreisi) = 23
Lai noteiktu protonu skaitu:
Protonu skaits vienmēr ir vienāds ar atomu skaitli, tāpēc X atomā ir 23 protoni.
Lai noteiktu elektronu skaitu:
Jons X ir pozitīvs (+3), tāpēc tas ir katjons, kas zaudējis trīs elektronus. Tātad tā elektronu skaits ir 20.
PIEZĪME: Elektronu skaita samazināšanās vai palielināšanās vienmēr notiek attiecībā pret atomu skaitli.
Lai noteiktu neitronu skaitu:
Neitronu skaitu nosaka, izmantojot masas un protonu skaitu šādā formulā:
A = p + n
51 = 23 + n
51 - 23 = n
n = 28
3. piemērs: Atoma W atoma skaitlis un masa ir vienāda ar attiecīgi 29 un 57, kas ir izobere no a atoms Y, kura atoma skaitlis ir vienāds ar 30, kas ir B atoma izotops, kura masas skaitlis ir 65. Izmantojot šo informāciju, nosakiet protonu, neitronu un elektronu skaitu atomā B.
Vingrinājuma sniegtie dati:
Atom W
atomu skaitlis (apakšā pa kreisi) = 29
masas numurs (augšējā labajā stūrī) = 57
Y izobārs, ti, Y masa ir arī 57.
Y atoms
atomu skaitlis = 30
masas numurs = 57
Ar šīm divām vērtībām mums jānosaka tā neitronu skaits, jo tas ir B elementa izotons:
A = Z + n
57 = 30 + n
57 - 30 = n
n = 27
B atoms:
masas numurs = 65
neitronu skaits = 27
Izmantojot šos datus, mums jānosaka tā atomu skaitlis, jo ar to mēs noteiksim tā protonu skaitu un elektronu skaitu (jo tas nav jons):
A = Z + n
65 = Z +27
65 - 27 = Z
Z = 38
Tāpēc atomā B ir 38 protoni, 38 elektroni un 27 neitroni.
* Viktora Rikardo Ferreiras domu karte
Ķīmijas skolotājs
Autors: Diogo Lopes Dias


