O aprēķins atomu masa elementa elements ir matemātiskais resurss, ko izmanto, lai noteiktu periodisko tabulu masas vērtību katram esošajam ķīmiskajam elementam. Kopumā, lai veiktu atomu masas aprēķins, mums jāzina šādi mainīgie ķīmiskais elements:
Elementu izotopi;
Katra elementa izotopa masas numurs;
Katra elementa izotopa procentuālais daudzums dabā.
Piemēram, ūdeņraža atoma masas aprēķins tika veikts, pamatojoties uz šādiem datiem:
Uzrāda protium izotopus (H1), deitērijs (H2) un tritijs (H3);
Šo izotopu masa ir attiecīgi 1, 2 un 3;
Protium procentuālais daudzums dabā ir 98,9%;
Deitērija procentuālais daudzums dabā ir 0,09%;
Tritija procentuālais daudzums dabā ir 0,01%.
Matemātiskais standarts atomu masas aprēķināšanai
Lai veiktu atomu masas aprēķins jebkura ķīmiskā elementa gadījumā mums jāizmanto šāds matemātiskais modelis:
1O: katra izotopa masas skaitli reizina ar tā procentuālo daudzumu;
2O: pievienojiet visus rezultātus, kas atrasti reizināšanas ar pirmo soli;
3O: daliet atrasto summu ar 100.
M.A. = masas numurs. procentos + masas skaitļos. procentos
100
Prāta karte: Atomu mise
* Lai lejupielādētu domu karti PDF formātā, Noklikšķiniet šeit!
Atomu masas aprēķināšanas piemēri
⇒ 1. piemērs: Sēra atomu masas aprēķins.
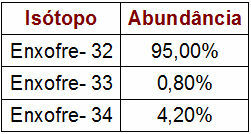
Sēra izotopu procentuālais daudzums un masas dati
Piedāvātajā tabulā norādīts katra sēra izotopa masas skaits un procentuālais daudzums dabā. Lai veiktu atomu masas aprēķinu, vienkārši veiciet šādas darbības:
1O Solis: reiziniet katra izotopa masas numuru ar tā daudzuma vērtību.
Sērs - 32 (S32)
s32 = 32.95
s32 = 3040
Sērs - 33 (S33)
s33 = 33.0,8
s33 = 26,4
Sērs - 34 (S34)
s34 = 34.4,2
s34 = 142,8
2O Solis: pievienojiet vērtības, kas konstatētas masas skaitļa un izotopa pārpilnības reizinājumā.
Summa = S32 + S33 + S34
Summa = 3040 + 26,4 + 142,8
Summa = 3209,2
3O Solis: aprēķina atomu masu, dalot atrasto rezultātu summu ar 100:
M.A. = Summa
100
M.A. = 3209,2
100
M.A. = 32,092 u
⇒ 2. piemērs: Dotajam ķīmiskajam elementam (D) ir trīs izotopi, kuru masas skaitļi ir:
30D 32D 34D
Zinot, ka šī elementa atoma masa ir 32,20 u un ka izotopa ir 20% 32D kāda ir pārējo izotopu procentuālā vērtība dabā?
Šis paziņojums norāda viena no izotopiem masas skaitļus, atomu masu un procentuālo daudzumu. Lai noteiktu citu izotopu procentuālo daudzumu, mums jāveic šādas darbības:
1O Solis: nosaka katra izotopa procentuālo daudzumu.
Izotops - 30 (DS30)
DS30 = 30.x
DS30 = 30x
Izotops - 32 (DS32)
DS32 = 32.20
DS32 = 640
Izotops - 34 (D34)
DS34 = 34.y
DS34 = 34g
2O Solis: lai aprēķinātu atomu masu, izmantojiet visus matemātiskajā izteiksmē atrastos datus.
M.A. = masas numurs. procentos + masas skaitļos. procentos
100
32,2 = 30x + 640 + 34g
100
32,2.100 = 30x + 640 + 34g
100
3220 - 640 = 30x + 34g
30x + 34g = 2580
x = 2580 - 34g
30
3O Solis: izmantojiet iepriekš minēto izteicienu no šāda pamatojuma:
Izotopa 1 procentuālā daļa + Izotopa 2 procentuālā daļa + Izotopa 3 procentuālā daļa = 100%
x + 20 + y = 100
x + y = 100 - 20
x + y = 80
x = 80 - y
2580 - 34g = 80-g
30
2580 - 34y = 30. (80. g.)
2580–34 g. = 2400–30 g
2580–2400 = 34–30 g
4y = 180
y = 80
4
y = 45%
4O Solis: aprēķiniet x procentuālo vērtību izteiksmē, kas izveidota trešajā solī.
x + y = 80
x + 45 = 80
x = 80 - 45
x = 35%
Autors: Diogo Lopes Dias
Avots: Brazīlijas skola - https://brasilescola.uol.com.br/quimica/calculo-massa-atomica.htm
