Pajėgumas, kurį jungtys turi pritraukti elektros krūviams, apibrėžiamas kaip poliškumas, kuris įgauna skirtingą pobūdį, priklausomai nuo ryšio, kuriame jis yra.
Kalbant apie joninį ir kovalentinį ryšį, pastaroji daro molekulę nepolinę. Molekulė, kurioje joninis ryšys yra atsakingas už atomų laikymą kartu, turi poliškumą.
Vyraujantis organinių junginių ryšys yra kovalentinis, todėl jie dažniausiai tampa nepoliniais junginiais. Ilgos anglies grandinės, esančios organinėse medžiagose, joms neleidžia nieko kito, išskyrus nepoliškumą.
Paaiškinimas kyla iš to, kad ryšys atsiranda tarp lygių elementų (Ç-Ç), todėl jie turi tą pačią elektronegatyvumo skalę. Žr. Pavyzdį:

nepolinė molekulė
Butanas, pavaizduotas aukščiau esančia struktūra, yra dujos, atkreipkite dėmesį, kad jungiamieji atomai yra vienodi (4 sujungiami anglies atomai).
Bet tai nereiškia, kad kiekvienas organinis junginys yra nepolinis, kitų anglies atomų buvimas suteikia molekulei polinį pobūdį. Peržiūrėkite pavyzdį:
Nesustokite dabar... Po reklamos yra daugiau;)
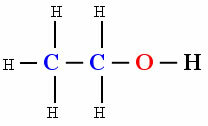
polinė molekulė
Hidroksilo buvimas Oi (Deguonis susietas su vandeniliu) organinio junginio etanolio molekulė parodė poliškumą.
Butanas naudojamas kaip žiebtuvėlių dujos, o etanolis yra vadinamasis įprastas alkoholis.
Autorius Líria Alves
Baigė chemiją
Brazilijos mokyklos komanda
Žiūrėti daugiau!
Organinių junginių savybės
Poliškumas – Sužinokite, kodėl elektronegatyvumas daro įtaką skambučio poliškumui.
Joninių ir kovalentinių ryšių poliškumas
Organinė chemija - Chemija - Brazilijos mokykla
Ar norėtumėte paminėti šį tekstą mokykloje ar akademiniame darbe? Pažvelk:
SOUZA, Líria Alves de. „Organinių junginių poliškumas“; Brazilijos mokykla. Yra: https://brasilescola.uol.com.br/quimica/polaridade-dos-compostos-organicos.htm. Žiūrėta 2021 m. Birželio 28 d.

