Pagal Pirmąjį termodinamikos dėsnį bet kuriame termodinaminiame procese šilumos kiekis Klausimas gaunamas sistemos yra lygus jos atliktam darbui ir vidinės energijos kitimui.
Kai slėgis yra pastovus, sistemos keičiama šiluma su išorine terpe naudojama darbui ir vidinei energijai pakeisti. Daugelyje praktinių situacijų sistemoms yra daromas atmosferos slėgis, kaip ir cheminės reakcijos atveju. Aukščiau pateiktame paveikslėlyje parodyta šio tipo proceso PV diagrama.
Šiuo atveju Pirmojo įstatymo lygtyje
Q = τ + ∆U
nė vienas iš terminų nėra nulis. Darbas parašytas kaip tūrio kitimo tūrio V funkcija, pavyzdžiui:
τ = P.∆V
Tam tikru idealių monoatominių dujų atveju energiją galima užrašyti taip:

Todėl mes galime parašyti Pirmąjį termodinamikos dėsnį kaip ΔV funkciją:


Šiluma, kurią keičiama su terpe, yra (5/2) P.ΔV, o 40% visos sumos, kuri atitinka P.ΔV, naudojama darbams atlikti; ir (3/2) P.ΔV, kuris atitinka 60% visos sumos, naudojami vidinei energijai pakeisti. Šis rezultatas galioja idealioms monoatominėms dujoms.
Šiluma yra susijusi su temperatūros kitimu (naudojant idealų dujų įstatymą):
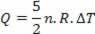
Taigi tiekiamą šilumą galima apskaičiuoti pagal temperatūros pokyčius arba pagal tūrį.
Autorius Domitiano Marquesas
Baigė fiziką
Šaltinis: Brazilijos mokykla - https://brasilescola.uol.com.br/fisica/primeira-lei-para-processos-isobaricos.htm
